文献解读
Nat Rev Mol Cell Bio | 小分子代谢物调控六大经典模式知多少?
提到“代谢”,大众的第一反应可能是“新陈代谢”,从宏观层面理解,也就是生物体内所发生的用于维持生命的一系列有序化学反应总称。这些反应进程使得生物体能够生长和繁殖、保持它们的结构以及对外界环境做出反应。从微观层面理解,代谢是细胞内发生的各种化学反应的总称,通常被分为两类:分解代谢即对大分子进行分解以获得能量(如细胞呼吸);合成代谢则利用能量来合成细胞中各个组分,如蛋白质和核酸等。而今天绘谱君提到的“代谢”是则是各类化学反应所涉及的小分子代谢物(分子量小于1000da),当然这些小分子代谢物根据来源可以分为外源性代谢物(药物或环境暴露物等)和内源性代谢物(糖类、氨基酸、脂肪酸等)。
为了检测这些小分子代谢物以及对这些小分子功能进行探索,逐步发展出“代谢组学“概念。发展了近30年的代谢组学涉及多个学科,主要包括分析化学、统计学、生物信息学、生物化学等。其中分析化学技术采用气相色谱-质谱联用技术(GC-MS)、液相色谱-质谱联用技术(LC-MS)和核磁共振技术(NMR)等对代谢物进行提取、分离、定性和定量检测;统计学方法用于处理和分析代谢组学数据,识别代谢物变化模式,揭示代谢反应的整体变化;生物信息学除了寻找对比组之间差异代谢物,还可以分析代谢通路和生物学功能;生物化学则有利于我们理解代谢物生物学功能。如今的代谢组学除了准确的对代谢物进行定性定量分析,更重要的任务是对筛选出的差异代谢物进行功能解析(这类代谢物可以称为生物活性代谢物或信号代谢物)。
绘谱君根据Nature子刊Nature Reviews Molecular Cell Biology(IF=81.3)上发表题为“Metabolites as signalling molecules”综述性文章为大家梳理代谢物如何调控细胞行为或机体行为。传统观点认为,代谢过程是被动适应以满足细胞的需求。然而,越来越多研究表明,代谢物不仅仅是为生物过程提供底物,还通过对代谢途径的影响或通过调节其他调节蛋白,以提供关键信号,比如参与营养感知和储存、胚胎发育、细胞存活和分化、免疫激活和细胞因子分泌等过程。这些研究表明,与目前流行的观点相反,细胞的生物化学由其潜在的代谢进行控制,而不是反过来。这一重要观点的转变,可以将常见代谢物视作为细胞(机体)表型和行为的关键调节因子。
代谢物调控细胞(机体)表型和行为经典方式包含以下6种,其主要机制是通过与大分子效应器(最常见的是蛋白质)的非共价结合来介导,也就是说这些代谢物与蛋白质相互作用感知众多小分子代谢物的丰度,从而调节它们的生成和消耗以实现代谢平衡。
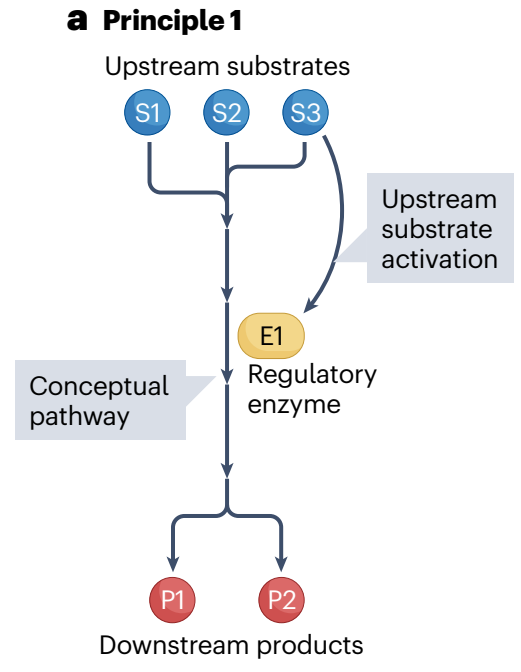
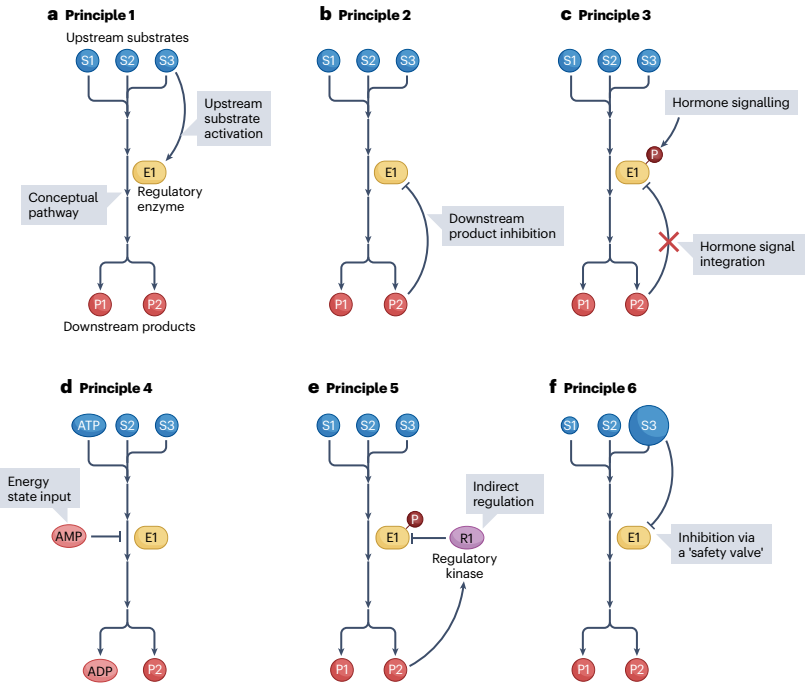
代谢调控模式一:此概念化代谢途径中包含三种底物(S1,S2和S3)和两种产物(P1和P2),其中一种酶(E1)催化该途径第三步。如果上游底物S3过度积累会激活通路中下游调控步骤,从而增加通路的通量,最终使代谢物浓度恢复到所需的范围内。
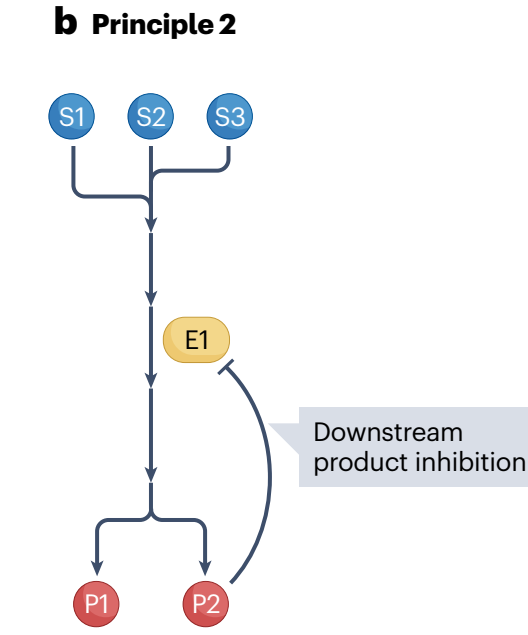
代谢调控模式二:与模式一相同代谢途径,如果下游产物P2过度积累通常会抑制通路中E1酶活性。
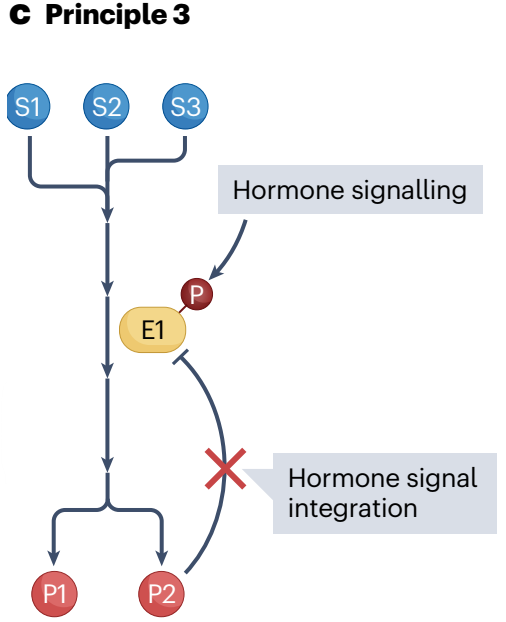
代谢调控模式三:调节酶通常可以接受激素信号的压倒性调节(如磷酸化,P),当生理条件需要通量时,尽管产物出现积累,但这些信号可以逆转下游产物抑制。
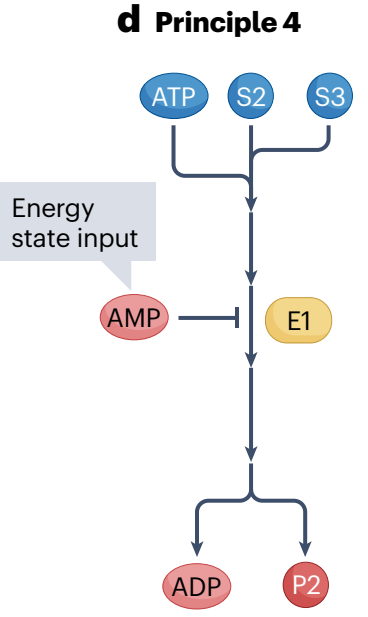
代谢调控模式四:此概念化代谢途径ATP(取代S1)并产生ADP(取代P1),从而消耗能量。当细胞能量水平严重耗尽时,低能量指标如AMP可以抑制调节酶。
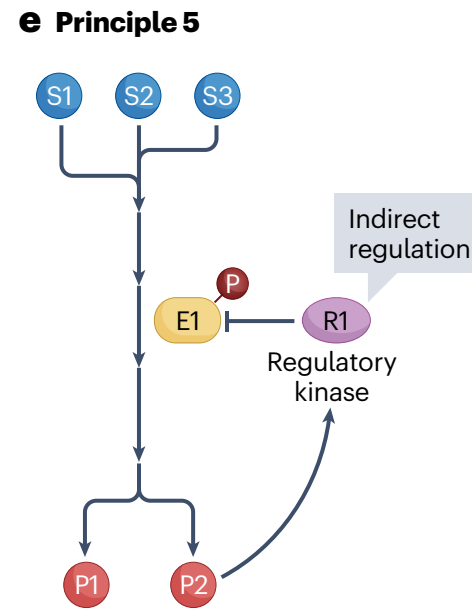
代谢调控模式五:在某些情况下,代谢物通过间接方式向通路中关键酶发出信号,如P2激活调节激酶R1来抑制E1磷酸化。
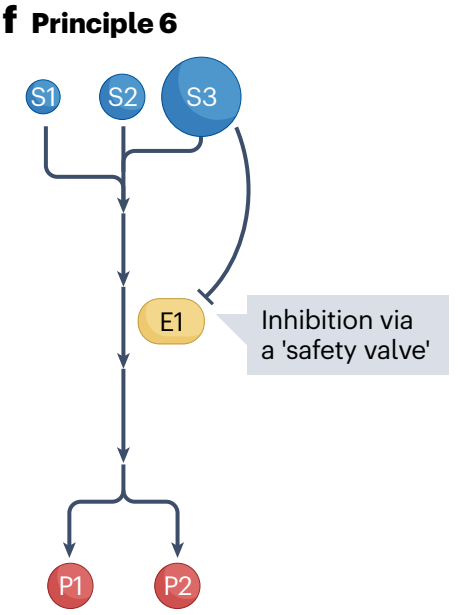
代谢调控模式六:一种底物(S3)过度积累可以通过质量作用推动代谢通量向前,从而导致其他底物(S1)的消耗,这可能是一种有害行为。为了防止有限底物耗尽,当其他底物水平较低时,过量底物水平也可以发出信号来抑制其消耗途径。
案例:葡萄糖代谢调节
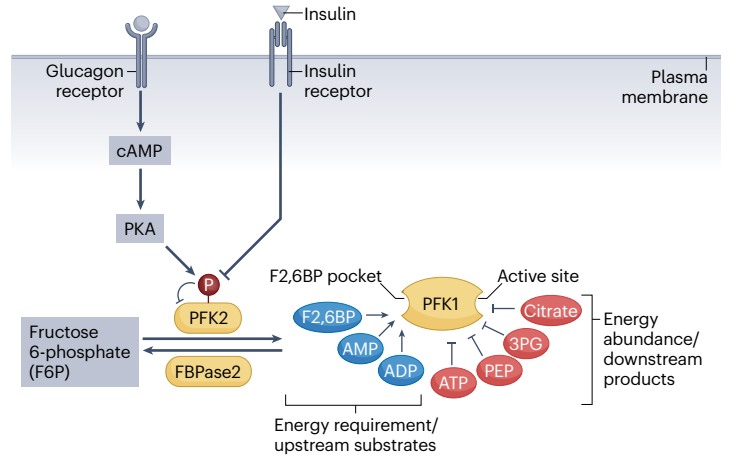
果糖6-磷酸(F6P)利用ATP被磷酸化成果糖1,6-二磷酸(F1,6BP)。尽管在磷酸转移过程中直接产生ADP,但糖酵解的总体结果是每消耗一个葡萄糖就净产生两个ATP。因此,ADP对磷酸果糖激酶1(PFK1)的激活可以作为模式一的一个完美案例,因为ADP是糖酵解上游“通路底物”,当积累到一定程度时,会刺激PFK1促进ADP到ATP的净转换。但PFK1也受到ATP以及糖酵解多种下游产物负调控,包括磷酸烯醇丙酮酸(PEP),3-磷酸甘油酸(3PG)和柠檬酸,体现为代谢调节模式二。重要的是,下游产物的积累,而不是它们的合成,抑制了上游催化反应。例如,当血糖高时,线粒体柠檬酸的正常生成导致其通过三羧酸(TCA)循环进行氧化代谢,而不会抑制PFK1。然而,在禁食期间,当脂肪酸氧化作为线粒体乙酰辅酶A替代来源时,柠檬酸会出现积累。然后柠檬酸被输出到细胞质,通过抑制PFK1来减少葡萄糖分解代谢,从而储存葡萄糖。
在代谢调节模式三中,PFK1可以被信号代谢物果糖2,6-二磷酸(F2,6BP)激活,F2,6BP是由磷酸果糖激酶2 (PFK2)合成。PFK2磷酸化F6P生成F2,6BP,并在多细胞动物中受到胰岛素和胰高血糖素通路调节。肝脏拥有一个高度复杂的代谢程序,一方面需要糖酵解协调代谢通量,另一方面通过相反途径(糖异生)来应对激素信号的协同调节。在空腹状态下,胰高血糖素(通常是对低血糖的反应)通过胰高血糖素受体(GL-R)激活蛋白激酶A (PKA)从而诱导PFK2磷酸化,导致PFK2失活,从而降低F2,6BP合成并抑制PFK1和糖酵解通量,最终使肝脏通过糖异生向其他组织供应葡萄糖。而在进食状态下,胰岛素信号通过蛋白磷酸酶2 (PP2A)介导去磷酸化激活PFK2,从而增加F2,6BP,进而激活PFK1增加糖酵解通量,即使在能量充足的状态下(ATP积累)也是如此。
在代谢调节模式四中,细胞能量充足和不足由几种途径感知和调节,以恢复能量稳态,从而确保细胞存活。与PFK1相对应的糖异生酶是果糖1,6-二磷酸酶(FBPase1)。FBPase1催化F1,6BP水解为F6P和磷酸盐,这逆转了PFK1在糖酵解过程中的催化反应,尽管没有再生PFK1消耗的ATP。虽然FBPase1和PFK1共享几个代谢物,但其传递的信号相反。例如,体外实验中AMP在100 μM浓度下激活PFK1超过6倍,反之抑制FBPase1。这确保了细胞的存活,因为AMP积累表明ATP形式的能量丰度降低,是一个危险信号。在一个正在进行糖异生作用但出现能量不足的细胞中,AMP可以阻止葡萄糖生成并推动糖酵解,使ATP浓度恢复到安全水平。
在代谢调节模式五中,以丙酮酸脱氢酶复合物(PDC)为例。丙酮酸通过糖酵解或由乳酸转化生成,也可以从氨基酸如丙氨酸代谢生成。它也可以通过发酵转化为乳酸或用于氨基酸合成,但其最典型功能是为线粒体TCA循环提供底物。丙酮酸由线粒体丙酮酸载体(MPC)运输到线粒体,经PDC氧化成乙酰辅酶A。PDC通过丙酮酸脱氢酶激酶(PDKs)的抑制性磷酸化间接接收代谢物信号。PDK2是脊椎动物中发现的四种PDK异构体中组织分布最广泛的,它被NADH和乙酰辅酶A异构激活,被ADP、NAD+、辅酶A(CoA-SH)和丙酮酸抑制。MPC-PDC系统控制着碳水化合物去向:氧化成二氧化碳;转化为其他细胞结构骨架;发酵。
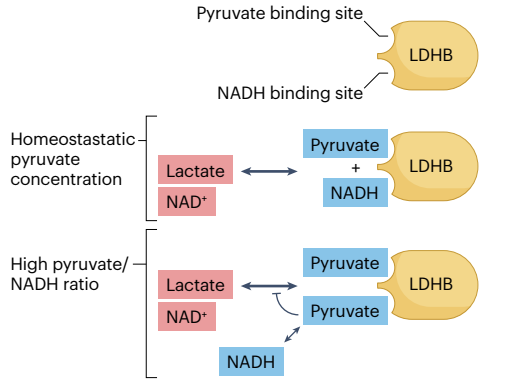
在代谢调节模式六中,代谢物信号可以作为一个“安全阀”防止细胞关键资源耗尽。例如,由于细胞内NAD+耗尽,NAD+/NADH比值降低会减缓糖酵解。当电子不需要转移到线粒体内分子氧时(在能量丰富条件下)或当这种转移受到缺氧限制(限制呼吸链活性),NADH将丙酮酸还原为乳酸,随后释放NAD+,这一过程是由乳酸脱氢酶(LDH)催化。脊椎动物表达四种乳酸脱氢酶异构体(A、B、C和D),但它们组织分布不同。在人类中,两种亚型占主导地位,其中LDHA在肝脏和骨骼肌中表达最高,而LDHB在心脏和大脑中表达更高。过量的丙酮酸都能抑制LDHA和LDHB,有趣的是,丙酮酸通过与NADH竞争结合来抑制LDHB。因此,该酶活性是由NADH与丙酮酸的相对丰度决定。当丙酮酸积累时,比如TCA循环停滞,乳酸的产生可能导致NADH过度氧化。通过竞争NADH结合,丙酮酸过量可能会限制细胞NADH的耗尽。
小结
在葡萄糖代谢过程中(糖酵解、TCA循环、糖异生)充分的体现了代谢调节的6个经典模式(底物-代谢酶-产物模式)。但代谢物的调控模式不仅仅这些,比如代谢物还以通过与蛋白质共价结合方式进行调控(蛋白质翻译后修饰),或者代谢物本身作为信号分子触发信号级联反应,或者代谢物在宿主与肠道菌群之间直接或间接传递信号信息。这些绘谱君将在后续内容中继续为大家梳理。
机体代谢网络复杂,围绕代谢物进行功能挖掘,需考虑几个开放性问题:
1)不同的生理状态下(比如不同饮食状态),代谢物如何变化?会有何种功能体现?
2)相同生理状态下不同组织部位(比如肝脏与肌肉),代谢物如何变化,有何种功能变化?
3)相同生理状态下相同组织部位不同细胞类型(比如肿瘤微环境中不同类型细胞),代谢物如何变化,有何种功能变化?
4)特定背景下,代谢物浓度水平不同,功能是否一致?
5)组织之间、不同类型细胞之间如何通过代谢物信号进行对话交流,影响彼此生物学功能?除此之外,还有很多问题值得各位深入探讨。
经典实验得出的代谢物信号原理
参考文献
Baker SA, Rutter J. Metabolites as signalling molecules. Nat Rev Mol Cell Bio. 2023;24(5):355-374.
请扫描二维码阅读原文
本公众号将持续针对代谢物调控模式以及结合相关研究案例进行梳理,以辅助理解代谢物自身如何代谢、代谢物如何通过相关调控模式影响机体表型更多代谢研究思路请持续关注收藏本公众号。
为了帮助大家针对自身领域开展深入的代谢物功能研究,麦特绘谱研发团队将多种相关分析、差异分析和网络分析方法进行高效整合,建立了多组学组关联分析的研究策略,已协助客户开展创新机制和干预靶点研究;同时我们推出一站式多组学-动物实验服务平台,多组学+动物验证无缝衔接加速探寻小分子代谢物功能与机制,详情请咨询客服或销售代表。
——绘谱君