文献解读
Nature Metabolism | 高蛋白饮食通过抵消乳酸菌的促进脂质吸收作用防止节食后脂肪量增加
肥胖,以其自身和增加的其它疾病风险,成为当前全球性的健康挑战;其根本原因是能量稳态的失衡。饮食限制(DR)或称节食,被认为是改善肥胖的有效策略——可能通过影响肠道菌群的组成和代谢来调节宿主新陈代谢。然而节食后恢复正常饮食后会往往会面临体重、体脂快速反弹的问题。目前学界对于这种情况下肥胖反弹的潜在机制、及如何预防这一过程的策略都不甚清楚。深入理解节食后体重体脂反弹的关键机制,并找到相应的干预策略对于肥胖的预防和治疗至关重要。

2022年12月1日,中国科学院上海营养与健康研究所翟琦巍研究组在国际知名期刊Nature Metabolism正式发表了题为“High-protein diet prevents fat mass increase after dieting by counteracting Lactobacillus-enhanced lipid absorption”的研究成果。该论文通过十种不同节食方式,研究了节食后身体脂肪累积反弹的潜在机制。研究结果揭示了肠道菌群(尤其是乳酸杆菌)产生的五种代谢物协同作用促进肠道脂质吸收和脂肪堆积——富含蛋白的饮食习惯可有效缓解这一过程,维持节食成果。同期,加州大学圣地亚哥分校胃肠病学系Amir Zarrinpar发表专评“A high-protein diet prevents weight regain”,赞赏了该研究成果。
节食后重进食会增强肠道脂质吸收、导致脂肪量增加
本研究通过5组短期饮食限制(SDR)小鼠模型,观察到取消SDR后脂肪含量和体重、腹股沟(iWAT)和附睾(eWAT)的大小及重量会显著反弹;使用苏木精和伊红染色iWAT和eWAT,发现脂肪细胞大小显著增加;肩胛间棕色脂肪组织(iBAT)肥大、脂滴增大、诱发肝脂肪变性。随后团队设计不同的DR实验验证了以上数据的可靠性。
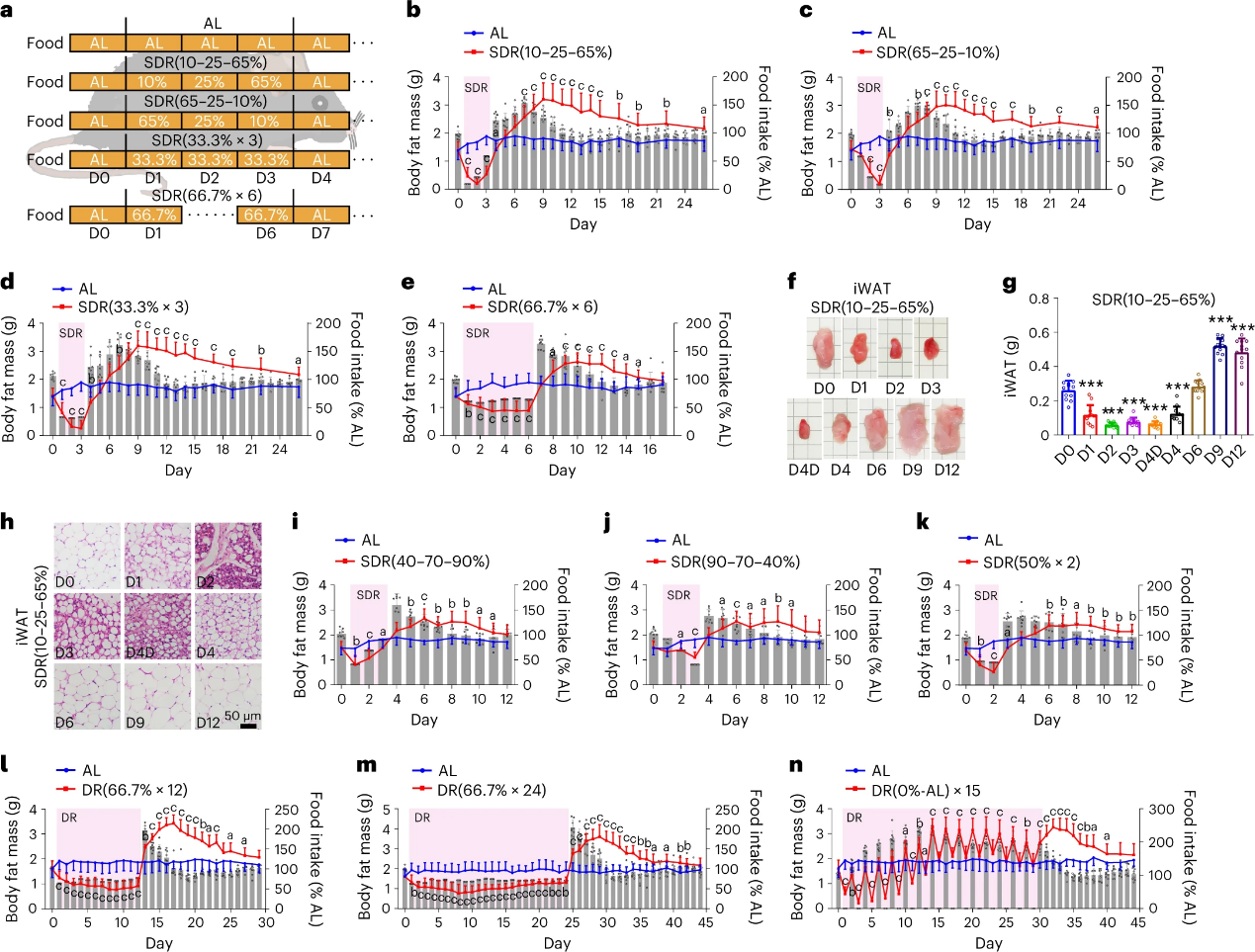
图1. SDR期间及取消后表型
团队通过调查,发现SDR后脂肪量快速积累不是由于能量消耗的减少;RT-PCR实验表明促进觅食基因(NPY、AgRP)mRNA表达量上升,厌食基因(POMC、CART)mRNA表达量下降。前面实验中,SDR组和对照组食物摄入量相当甚至更低,结合SDR组(10-25-65%、33.3%*3)实验结果,证明食物总摄入量或取消SDR头几天的进食不是脂肪快速累积的主要原因。
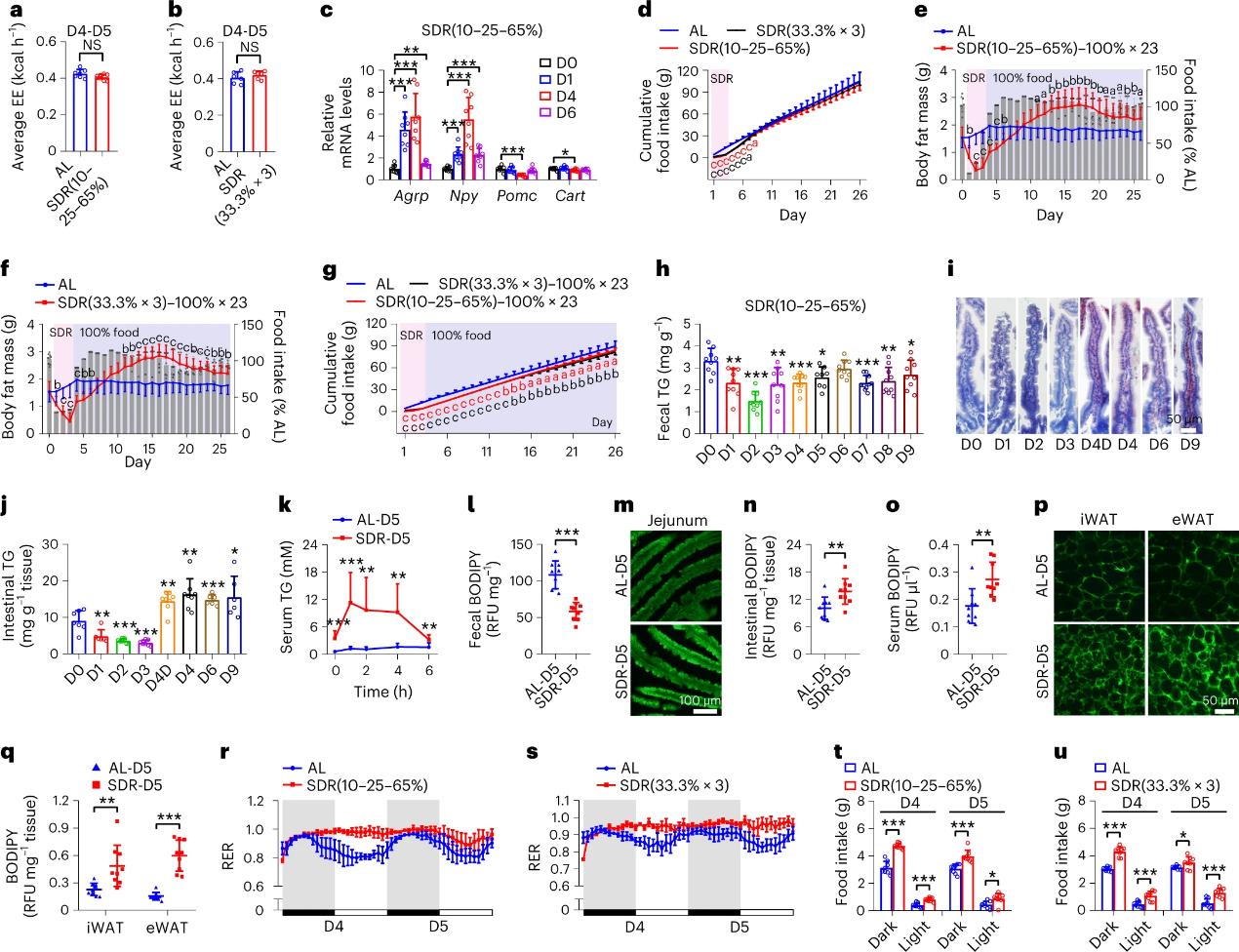
图2. SDR后再进食上调肠道脂质吸收
为探究SDR后脂肪量快速积累的机制,团队尝试探究肠道菌方向——SDR(10-25-65%)小鼠粪便甘油三酯(TG)显着降低;小肠绒毛的油红O(切片)染色和小肠TG定量均表明,SDR后小肠中TG明显增加。BODIPY标记脂肪酸与橄榄油结合的管饲法实验及相关定量实验进一步证实上述结果——SDR后粪便BODIPY水平显着降低,近端空肠绒毛切片的荧光强度显着增加。这些结果表明肠道脂质吸收增强有助于SDR后脂肪量的快速积累。
随后,团队通过BODIPY标记脂肪酸的管饲法发现SDR后再喂养会增加WAT中的脂肪酸摄取;高通量RNA测序发现SDR后脂肪酸和TG合成显着增加,呼吸交换比增加(总脂质氧化减少),食物摄入显著增加,表明WAT中脂肪酸摄取和脂质合成的增加,总脂质氧化的减少有助于SDR后脂肪量的快速积累。
高蛋白饮食减弱肠道脂质吸收、阻止脂肪增加
为了寻求有效的措施防止SDR后的脂肪增加,团队对SDR前中后三个阶段的血清进行了非靶向代谢组学——差异血清代谢产物主要集中在蛋白质消化吸收、氨基酸代谢合成途径。基于液质联用的靶向定量分析表明在SDR期间和之后,必需氨基酸(EAA)显著增加。通过独立SDR实验,团队发现SDR(10-25-65%)后分别补充高中低含量蛋白(HP、NP、LP)、NP+EAA都有助于防止脂肪快速积累,尤其是HP——iWAT和eWAT的大小和重量、H&E染色结果、iBAT肥大及其脂滴的积累被阻止、肝脂肪变性被抑制进一步证实该结果。并且,团队进一步通过SDR(33.3%*3、66.7%*12、10%–25%–65%)后+HP实验证实上述结论。
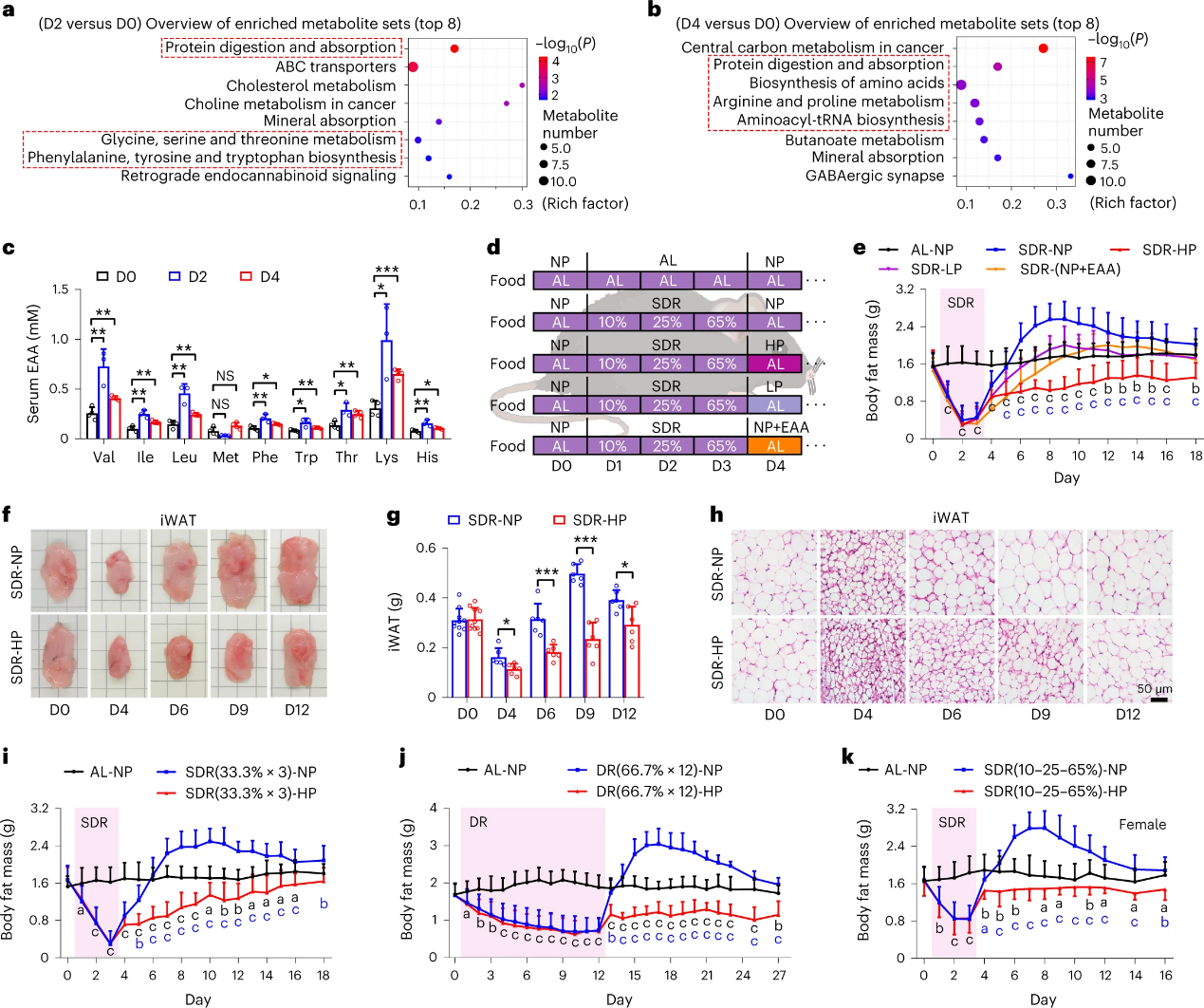
图3. 高蛋白饮食有效阻止节食后脂肪反弹
研究人员发现,SDR后喂食HP组降低了能量消耗,表明HP组脂肪累积抑制不是由于能量消耗。相比于NP,HP组日摄食量相当而总摄食量显著少于NP组。团队进一步改变小鼠SDR后的饮食,发现饮食结构类型会明显影响SDR后的脂肪累积,而不是总热量摄入。
定量结果显示,相比于NP组,HP组小鼠粪便TG和盲肠粪便总长链脂肪酸(LCFAs)均显著增加;相比于正常组,NP组小鼠肠道和血清总胆汁酸(促进脂质吸收)的增加而HP组显著降低。与此一致,BODIPY标记脂肪酸与橄榄油结合的管饲法、BODIPY标记脂肪酸管饲的小鼠中近端空肠绒毛切片及直接定量数据均显示,NP组与HP组指标相反。结合高通量测序数据,团队表明,SDR后喂食HP引起的脂肪增加抑制,源于WAT脂肪酸摄取和脂质合成减少以及总脂质氧化增加。
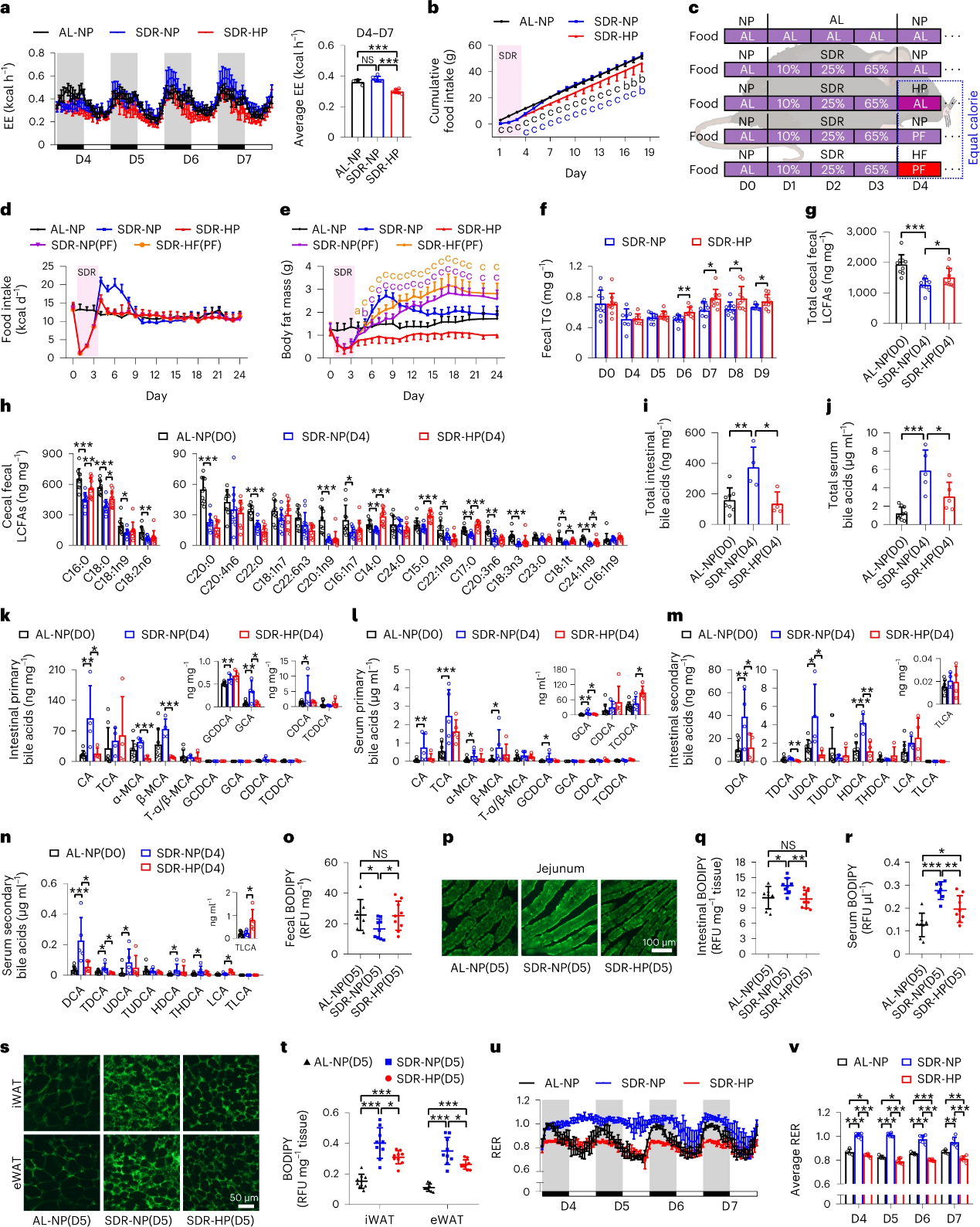
图4. 高蛋白饮食降低肠道脂质吸收
肠道乳酸杆菌促进肠道脂质吸收并增加脂肪量
为了探究肠道菌是否参与这一过程,研究人员对SDR(10%-25%-65%)+蛋白喂养的小鼠盲肠粪便进行16S测序分析。相比于正常组,NP组α多样性分析中乳酸杆菌属的显著增加并高于HP组。进一步,团队在第4天从SDR(10-25-65%)组小鼠的盲肠粪便分离并测序了8个菌落,基于系统发育树将其中一个被命名为Lam-1。qPCR定量证实Lam-1丰度因NP饮食增加,被HP饮食抑制。相比于正常组,使用抗生素消耗肠道菌的小鼠肠道脂肪酸吸收、WAT中的脂肪酸摄取显著降低,抑制了食物摄入量和脂肪量百分比的增加以及瘦体重百分比的降低。团队发现,使用青霉素后能显著抑制Lam-1丰度而不影响其余总体肠道菌,显著降低再喂养期间小鼠肠道脂肪酸吸收和iWAT脂肪酸摄取、显著改善脂肪量积累、抑制脂肪量百分比的增加和瘦体重百分比的降低。这些数据表明,SDR后再进食是通过肠道微生物群促进脂肪量积累、肠道脂质吸收、WAT的脂肪酸摄取。
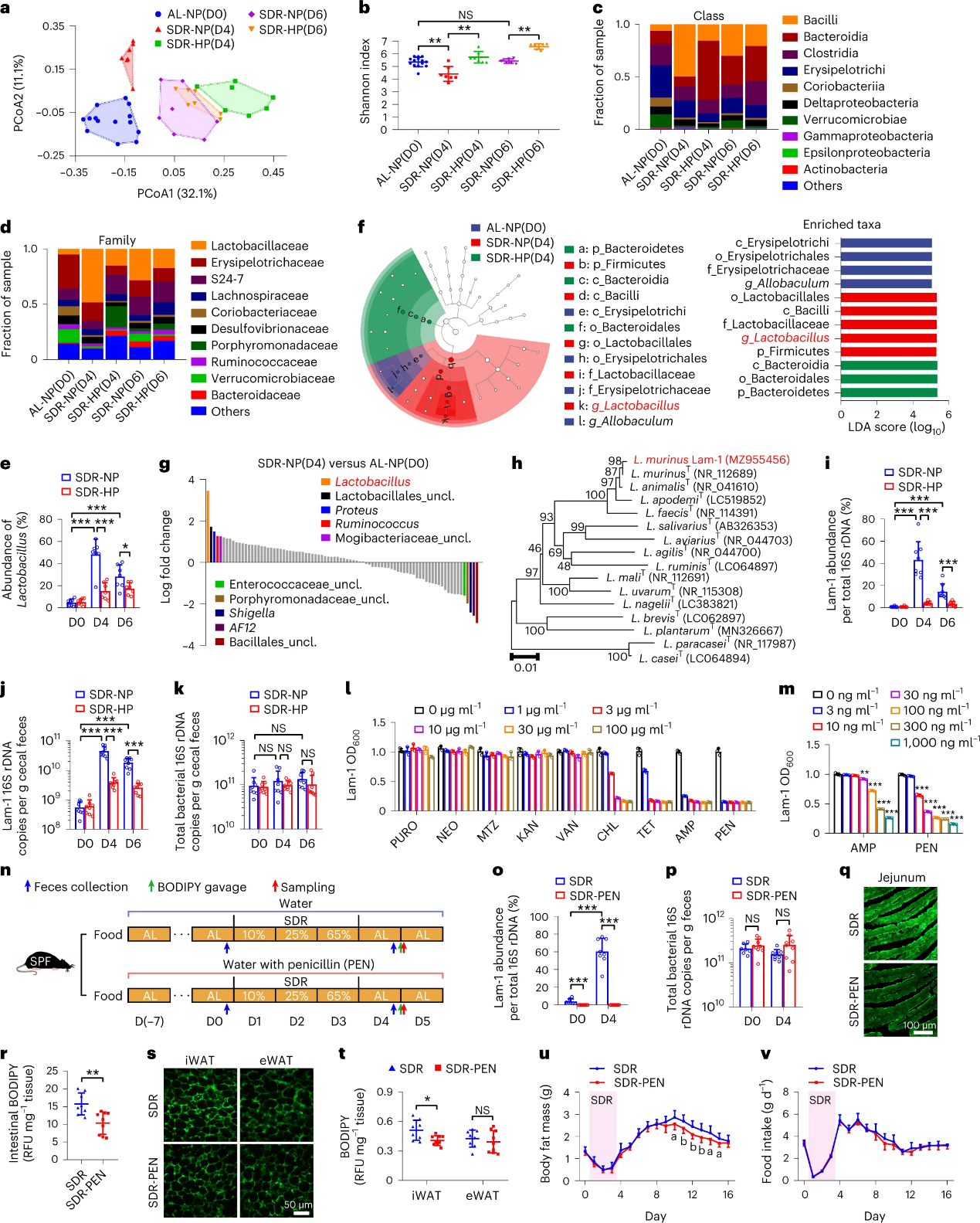
图5. SDR后再进食改变肠道菌群组成并影响肠道脂质吸收
团队将盲肠粪便转移至SPF级小鼠,与预期一致,在SDR-NP组菌群转移的受体中,肠道脂质吸收和脂肪酸摄取显著高于SDR-HP组。相比于副干酪乳杆菌(LC2W),灌胃Lam-1组的无菌小鼠WAT中肠道脂质吸收和脂肪酸摄取、eWAT的重量显著增加。接着,团队使用小鼠肠道中主要细菌门成员的八种细菌,对SPF级小鼠进行定菌移植;分别使用Lam-1和LC2W对定菌小鼠进行灌胃,结果显示,Lam-1组增加iWAT中的肠道脂质吸收和脂肪酸摄取,提高了iWAT和eWAT的重量。独立的SPF小鼠灌胃协同BODIPY标记脂肪酸实验,同样表明了Lam-1的促脂肪累积效果,而不会改变食物摄入量。这些结果表明,SDR后再喂养Lam-1可以增强肠道脂质吸收,增加WAT中脂肪酸的摄取并诱导脂肪量积累。

图6. Lam-1增强肠道脂质吸收和WAT脂肪累积
乳酸杆菌代谢物增加肠道脂质吸收和脂肪量
使用AB Sciex Triple TOF 6600对不同时间点和不同组小鼠的血清和粪便进行非靶向代组学分析,结果表明,SDR+NP组的代谢特征明显区别于随意喂养组,并通过HP饮食被部分阻断。在这部分可阻断致升高类物质中,DL-3-苯基乳酸(PLA)、4-羟基苯乳酸(HPLA)、2-羟基异己酸(HICA)、2-羟基-3-甲基丁酸(HMBA)和吲哚乳酸(ILA)在SDR+NP组中排名前5;随后使用安捷伦4000 Q-Trap靶向确认了这5种物质的趋势改变。Spearman相关性分析表明,乳酸杆菌与盲肠粪便中这5种物质水平的相关性最强;乳酸杆菌Lam-1强饲也表明盲肠粪便中这5种物质含量升高。进一步靶向检测细菌代谢物,Lam-1中这5种物质含量远高于LC2W和大肠杆菌。团队进一步分别使用5种物质单体或混合物、水、谷氨酸、葡萄糖进行强饲,结合BODIPY标记脂肪酸、生理指标测定等实验,证实只有5种物质混合才具有促进脂肪累积效果,并绘制本研究相应机制图。
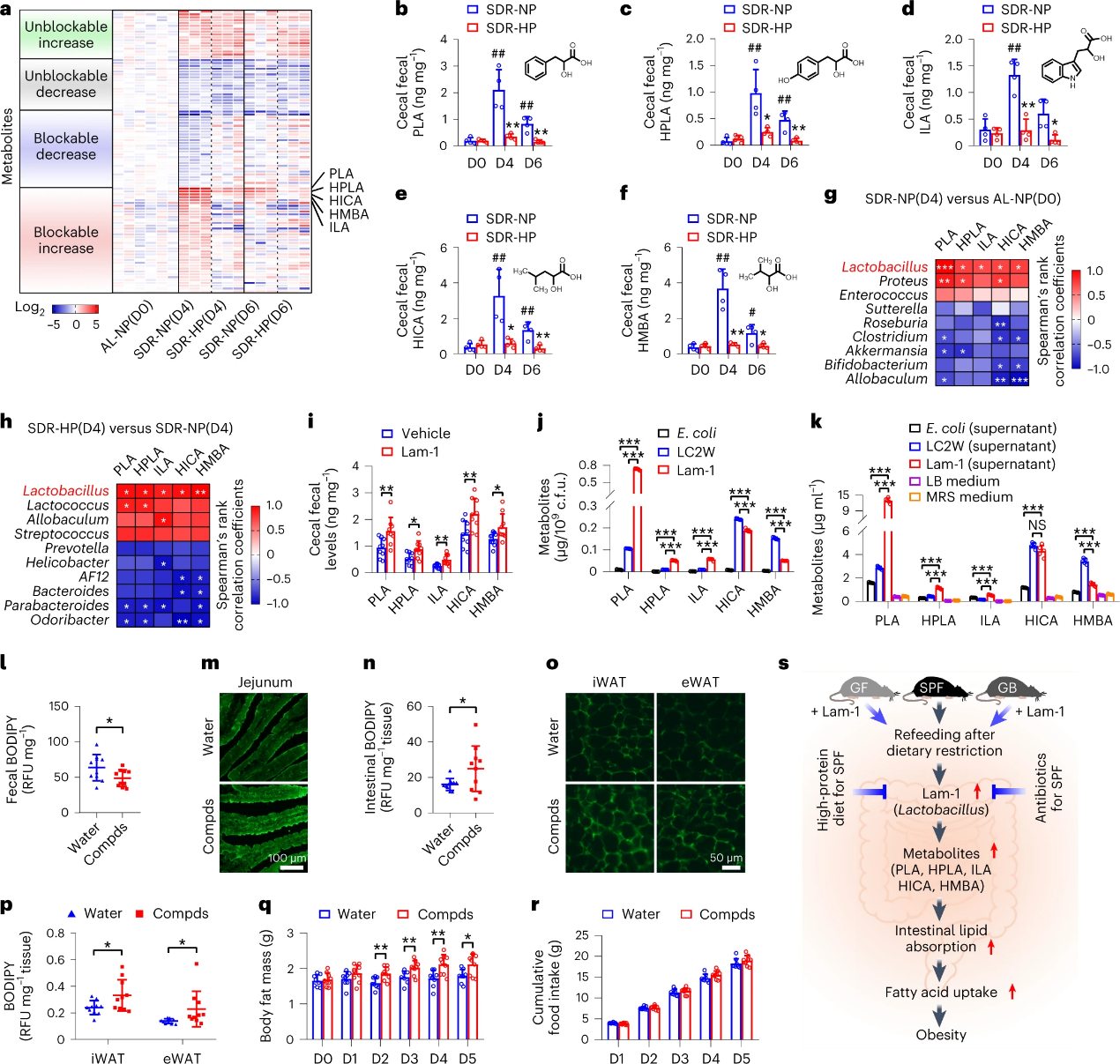
图7. SDR后再喂养调节菌群代谢物,增强肠道脂质的吸收及脂肪积累
小结
肥胖给人类带来诸多危害,本研究着眼于肥胖的根源——能量稳态失衡,揭示解除饮食限制后身体脂肪累积反弹的潜在机制。通过控制小鼠饮食方式,发现节食后重进食会导致脂肪量快速积累导致肥胖。结合生理指标、非靶向及靶向代谢组学发现高蛋白饮食有助于控制脂肪累积;利用16S测序、抗生素消耗菌群、菌群移植等方法,最终锁定到关键肠道菌Lam-1——Lam-1增强肠道脂质吸收,促进脂肪堆积,该过程可被高蛋白饮食抑制。利用非靶向代谢组学结合相关性分析锁定5种菌群代谢物,并通过靶向代谢组学验证了组间趋势。进一步通过小鼠节食实验,表明肠道菌群(尤其是乳酸杆菌Lam-1)产生的这5种物质同时存在时才能上调肠道脂质吸收,诱导脂肪积累致肥胖。总之,研究团队的工作为通过微生物控制人体脂肪累积,或改变饮食方式维持健康身材提供了深入的理解。
参考文献
High-protein diet prevents fat mass increase after dieting by counteracting Lactobacillus-enhanced lipid absorption. Nature Metabolism. 2022.
请扫描二维码阅读原文

绘谱帮你测
上述研究通过非靶向/靶向组学和粪便16S测序结合,经过大量数据发掘和10种节食方式等体内实验探究并验证节食后脂肪累积与肠道菌群之间的潜在机制。随着肠道菌群研究的深入,菌群与宿主代谢相互作用日益成为热点,麦特绘谱拥有业内强大的Q600全定量代谢组、Q300全定量代谢组、Q200宏代谢组检测平台,菌群16S测序和宏基因组等技术,适用于包括粪便/肠内容物等样本的分析,提供代谢组学一站式整体解决方案,独家的检测技术、全面的数据报告以及专业的售后探讨,已经协助客户完成多个肠道菌群代谢相关项目,发表在Cell Metabolism, Gut, Science Translational Medicine, Diabetes Care, Microbiome等顶级期刊,总影响因子超过2000。麦特绘谱助力您的科研探索之路不断创新和突破,详情请咨询绘谱热线400-867-2686,获取详细资料!
往期推荐
3. Nature | 间歇性禁食通过肠道代谢产物3-吲哚丙酸促进神经再生和修复
4. Nature Medicine | 临床大队列代谢组&基因组探究代谢个体差异的遗传因素
5. Cell Metabolism | 运动代谢图谱揭示代谢稳态的时间依赖性特征
6. Cell Metabolism重磅综述 | 肠-肝轴的病理生理学概念和临床意义(下)



