文献解读
Cell︱多组学研究急性运动对机体的分子调控
适当体育运动有益于提高机体免疫力、增强心肺功能、改善认知能力并调节身体代谢水平等等。而急性体育运动会触发急性炎症标志物(如白介素-6)和代谢途径(如糖酵解和脂肪酸氧化)变化等复杂的分子反应。对此美国斯坦福大学医学院Michael P. Snyder等研究团队报道了急性运动后分子层面的系统变化,通过对受试者运动前后的血浆和外周血单个核细胞进行纵向多组学(包括代谢组、脂质组、免疫组、蛋白质组和转录组)的时间序列分析,揭示了成千上万的分子变化和生物过程的重编排,涉及能量代谢、氧化应激、炎症、组织修复和生长因子反应等,相关研究成果发表于《Cell》杂志。
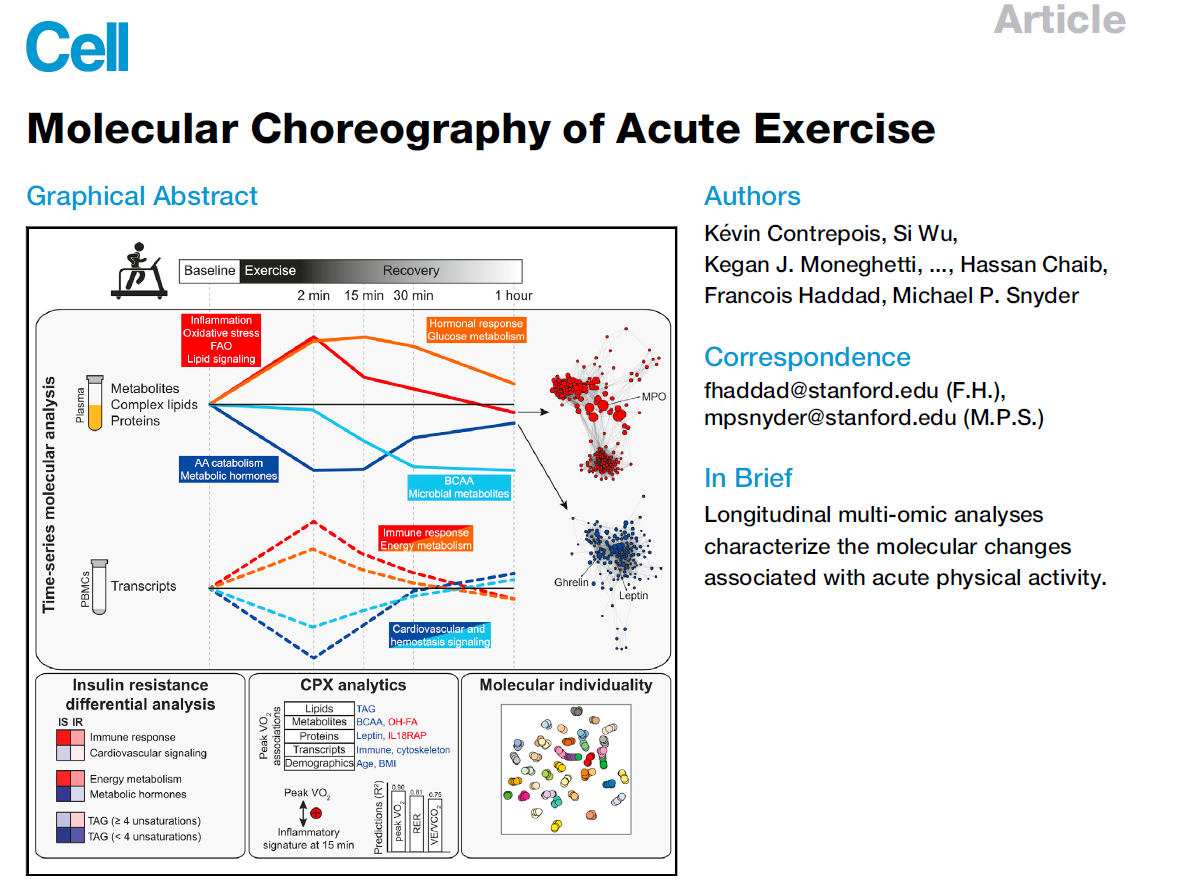
急性运动后的多组学变化
研究人员采集36名参与者在运动前(基线)和运动恢复2 min、15 min、30 min和1 h后静脉血,其中15名参与者提供次日空腹血样以评估日间血液的差异,此外,纳入14名作为对照组。随后进行血浆靶向和非靶向蛋白组学、非靶向代谢组学、半定量脂质组学以及外周血单核细胞(PBMCs)转录组学分析,共获得17662个分析物,分别为15855个转录本、260个非靶向蛋白、109个靶向蛋白、728个代谢物和710个复杂脂质。上述纵向多组学数据集被用于:
(1)筛选急性运动的动态分子反应;
(2)确定与VO2峰值相关的分子并预测运动生理学的关键指标;
(3)分析胰岛素抵抗参与者对运动的差异反应;
(4)在个体水平分析异常值的临床相关性。
对个体基线、年龄、性别、种族和BMI校正后确定了运动对分子的显著影响,发现急性运动引起9815种分析物发生广泛变化(图1C)。不同分子类型观察到不同的变化模式,转录本反应非常迅速,运动后早期达到最高/最低水平,且在60分钟内回到基线,而442个代谢物和192个脂质在整个过程都发生了改变,其中19.5%和28.9%在60分钟恢复期内仍存在显著差异。根据对照组数据分析表明,这些变化是受运动影响,而非分析物或禁食的自然变化所影响。此外,运动的分子反应水平比个体日间变化至少大2倍。个体基线与个体对运动响应程度存在不同,基线时,复杂脂质的变异系数(CV)最高,其次是代谢物、蛋白质和转录本,分别为62.0%、46.2%、38.9%和26.9%。而运动后,蛋白质变化最大CV为 36.8%,其次是代谢物、转录本和脂质分别为32.1%、27.7%和17.0%(图1E)。与运动相关最易变的转录本(n = 1,334)富集到了骨关节炎和肝纤维化/肝星状细胞活化途径,表明这些通路对运动响应中的差异调节。
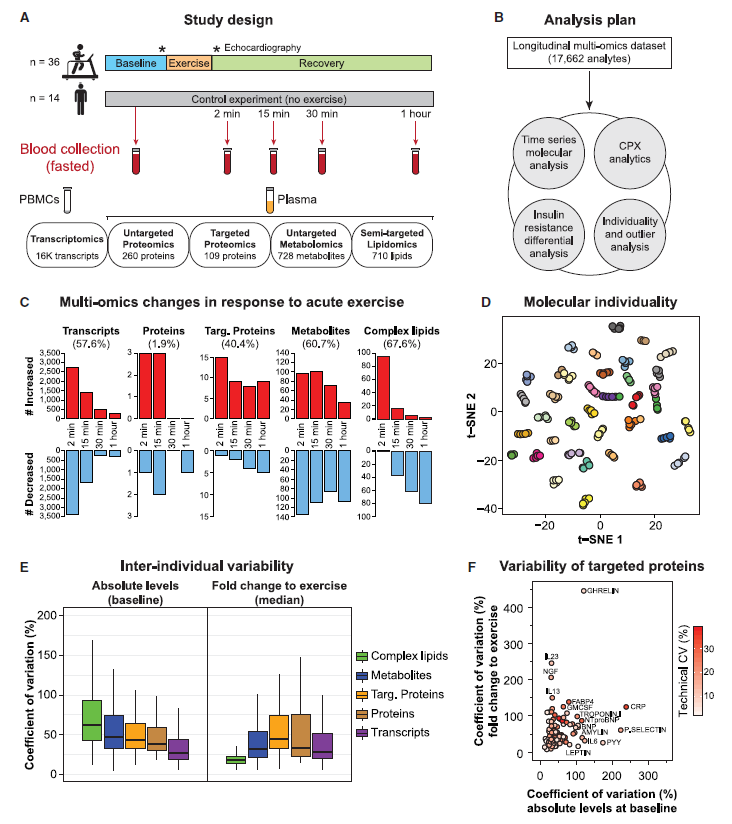
图1 试验设计、运动的分子反应以及个体间差异
全系统时间序列分子分析
研究人员对运动后的高密度采样进行c-means聚类,将变化的物质分为4个簇,描述了早期(即能量代谢、氧化应激和免疫反应)和晚期(即能量稳态、组织修复和重塑)的关键生物过程(图2A)。
Cluster 1:在运动后增加并迅速回到基线,与厌氧代谢、免疫反应、氧化应激、脂肪酸氧化和脂质代谢相关。正如预期,血浆中糖酵解产物(如乳酸、丙酮酸)和TCA循环中间体(如苹果酸)急剧增加,反映厌氧代谢增加(图2B)。运动后炎症反应通过分泌IL-6和肿瘤坏死因子α(TNF- α)而表现明显(图2C)。内皮标记物和血管粘附分子也与血管细胞粘附分子-1 (VCAM-1)、E选择素和内皮细胞特异性分子1 (endocan 1)也成为Cluster 1的关键分子。许多酰基肉碱和游离脂肪酸的早期积累表明脂肪酸氧化(FAO)是由运动激活的,中链酰基肉碱(如C6:0, C8:0, C10:0和 C12:0)随着运动而累积最多,并在运动后15-30 min内回到基线,其他酰基肉碱(如C6:1, C8:1, C14:0和 C16:1)累积较少,且恢复到基线速度较慢(30 min-1 h)(图2E, 2F)。游离脂肪酸表现出三种主要的运动轨迹,其中一些在运动后2分钟达到最大值(10-12个碳,Cluster 1),一些在15分钟达到最大值(14-18个碳,Cluster 2),其余的在恢复2分钟时减少(20-24个碳,Cluster 3)(图2F)。这些结果在差异表达分析证明,20-22个碳的长链脂肪酸(C20:1、C20:2、C22:1、C22:2、C22:3)在运动过程中被优先氧化。此外,运动还伴随着多种脂质的短暂积累,包括胆固醇酯(Ce)、磷脂酰胆碱(PC)、二酰甘油(DAG)、神经酰胺(Cer)和鞘磷脂(SM)(图2D)。
Cluster 2:运动后某些分析物回落至基线前出现延迟增加,与碳水化合物代谢、类固醇、皮质类固醇和肾上腺激素等分泌有关。相关性网络发现皮质醇的增加,可以刺激肝脏葡萄糖异生,导致循环葡萄糖水平上升,葡萄糖和胰岛素水平存在显著正相关,胰岛素是Cluster中最相关的蛋白质组特征物质。葡萄糖代谢增加与TCA循环成分(苹果酸、柠檬酸、α-酮戊二酸)相关,导致腺嘌呤核苷酸分解代谢产物(如次黄嘌呤和黄嘌呤)显著增加,这是ATP周转率的标志物(图2B)。此外,凝血和止血因子出现增加。
Cluster 3:随运动而减少,1小时内回到基线,相关性网络以瘦素和胃饥饿素为中心,表明运动可调节食欲(图3)。运动时15个氨基酸水平发生变化,反映了运动生理学中的核心作用(图2E)。Cluster 3中的六种氨基酸(谷氨酸、胱氨酸、色氨酸、丝氨酸、苏氨酸和甘氨酸)可能被骨骼肌细胞分解产生能量并在恢复阶段重新合成。Cluster 2中四种氨基酸(丙氨酸、酪氨酸、谷氨酰胺和脯氨酸)呈现相反轨迹,这是细胞代谢增加的产物。
Cluster 4:运动后继续减少,1小时内没有恢复到基线,支链氨基酸(BCAAs)亮氨酸、异亮氨酸和缬氨酸优先被骨骼肌分解(图2G),用于修复受损的骨骼肌纤维。此外,微生物代谢物(图2H)、异生物质(咖啡因代谢)和胆汁酸有着相同的代谢轨迹。Cluster 1中三酰基甘油(TAG)含有的脂肪酸比Cluster 4中TAG的碳更多且更不饱和(图2I)。总之,密集抽样揭示了TAG的动态和功能上不同的子类。
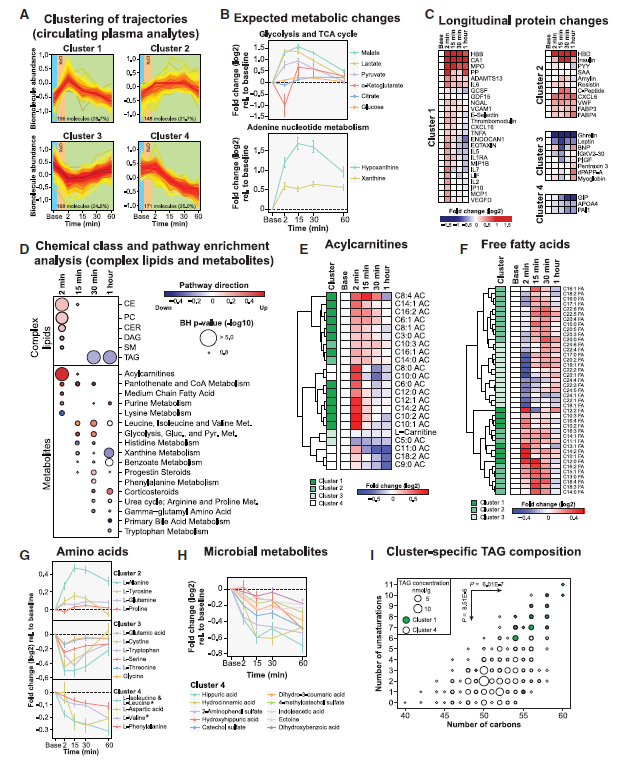
图2 急性运动的多组学变化
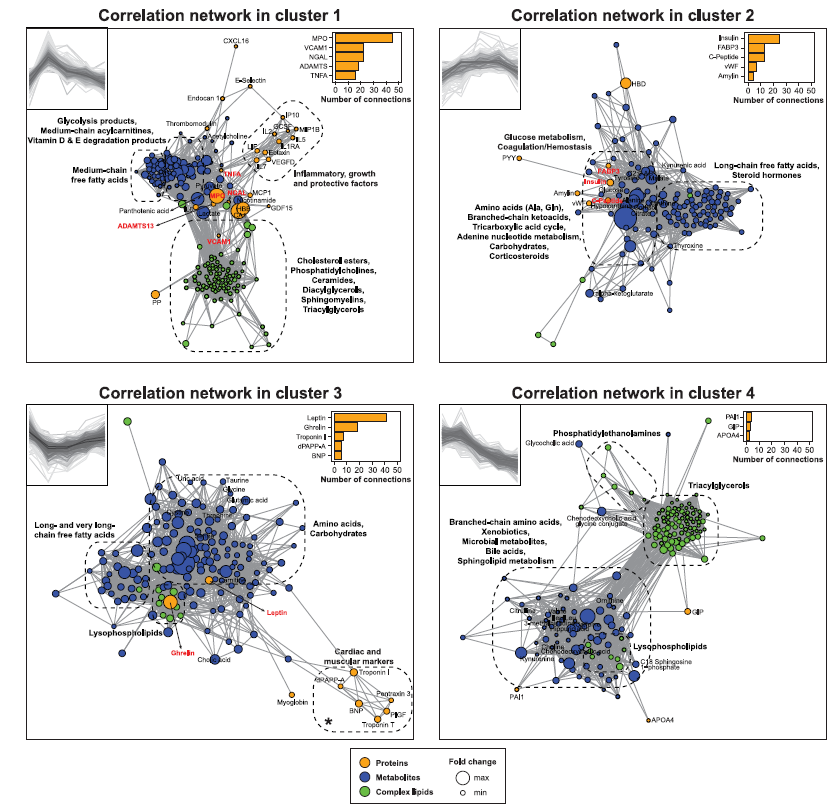
图3 循环分析物的综合多组学分析
时间序列PBMC基因表达分析
研究人员对PBMC基因表达进行了分析,以明晰免疫系统随运动的变化,发现上调和下调基因在2 min 达到最大,在30-60 min 迅速恢复到基线(图4A)。富集结果表明,免疫系统被激活(图4B),与炎症反应相关的自然杀伤细胞、Th1和Th2活化、B细胞受体、T细胞受体、核因子κB信号以及许多白细胞介素信号通路的表达均显著增加;还有许多与细胞生长和移动相关的通路也被上调,可能参与肌肉组织修复和重塑。此外,一些与心血管和止血相关的信号通路也发生改变,突出了运动与心血管健康的相互关联。运动可以影响免疫细胞的数量且与细胞类型有关。因此,基因表达的变化可能通过细胞突变和细胞激活的结合而发生。
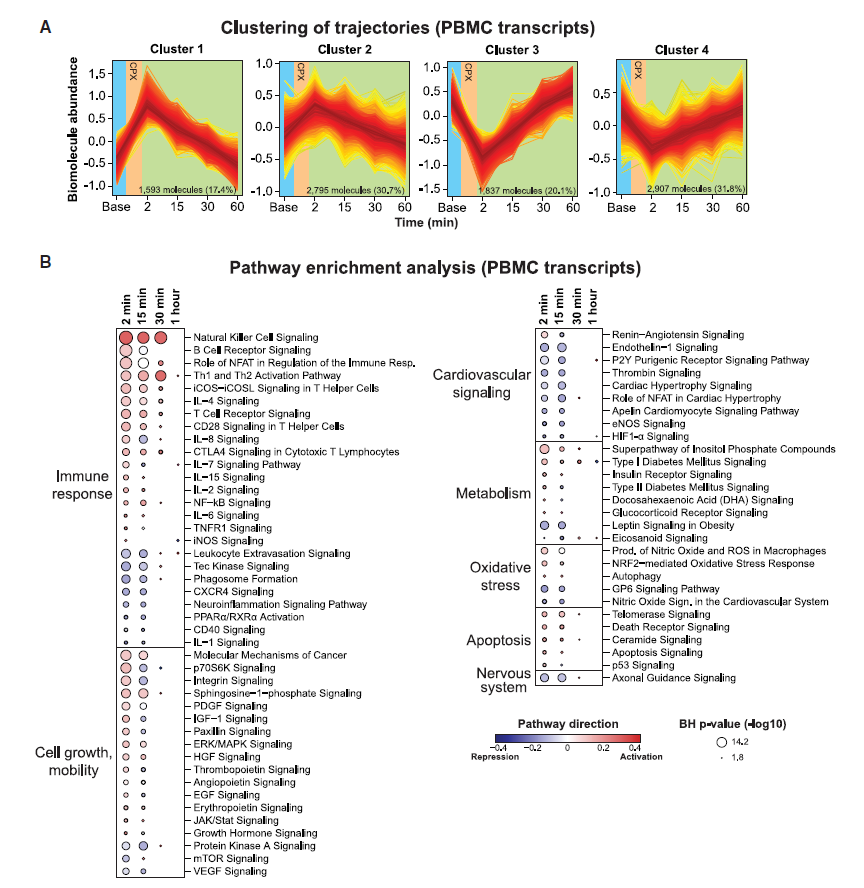
图4 急性运动对PBMC基因表达的影响
心肺运动(CPX)参数的多组学特征
CPX参数对一般人群、心血管和代谢性疾病患者的结果具有很强的预测作用。最大耗氧量(峰值VO2)是一般人群寿命和心力衰竭患者生存率的最佳预测指标之一。应用线性回归模型发现基线和恢复期每个时间点的VO2峰值存在显著相关性,观察到大部分组学指标(51.9%的复杂脂质和30.3%的代谢物)与运动能力显著相关。在恢复早期(2-15 min),最强的关联是与葡萄糖、苹果酸、柠檬酸、乳酸、低黄嘌呤和黄嘌呤等能量代谢相关分子的正相关,以及与色氨酸、胱氨酸、鸟氨酸和尿囊素的负相关(图5B);在恢复后(30 ~ 60 min),皮质醇呈正相关,长链、多不饱和游离脂肪酸和中链的肉碱呈负相关,这突出了能量稳态的重要性。此外,IL-5(运动后15 min与其相关的蛋白数量最多)和TGF-β(可能参与调节适应度炎症信号)可能导致适应性炎症特征。除了多组学数据,还将临床指标和肠道微生物组数据纳入贝叶斯网络算法和Ridge回归模型筛选高预测分子,建立峰值VO2、VE/ VCO2和RER的预测模型,发现在峰值VO2模型中添加组学数据能显著提高模型的性能(图5G),并筛选到瘦素、血糖、肠道Butyricimonas属和血浆中的二十碳五烯酸(EPA)等预测分子(图5)。
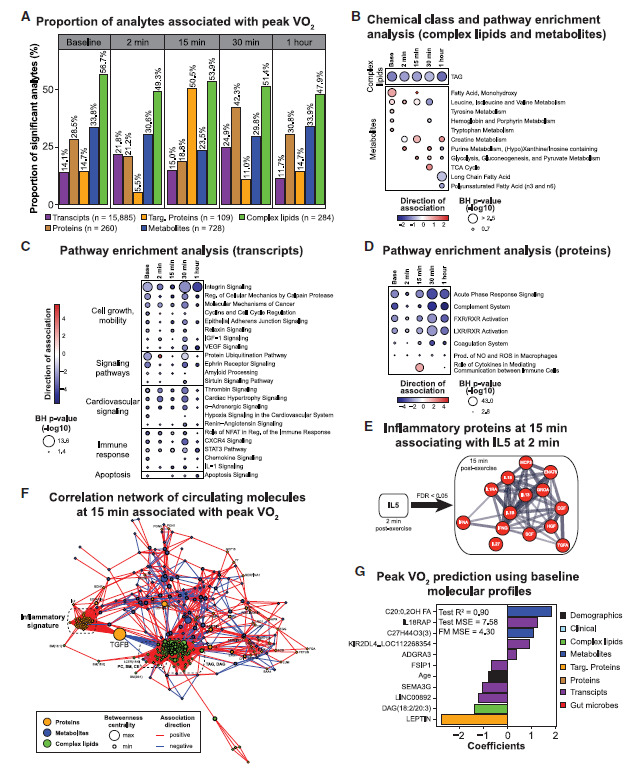
图5 峰值VO2多组学分析
胰岛素抵抗患者对运动的差异应答
本研究中所召募的志愿者中胰岛素抵抗病人占有相当的比例,因此研究人员还比较了胰岛素抵抗(IR,n=16)与胰岛素敏感(IS,n=14)两组人群之间的差异应答分子。使用线性混合模型调整个体基线、年龄、性别、种族/民族和BMI,在所有组数据中发现了2279个差异分析物,并根据其纵向轨迹分为6个不同的时间序列模式:模式1和模式2分别在IS和IR受试者中为高幅度的上调分析物,模式3和模式4为下调分析物,模式5和模式6为相反的轨迹。
通路富集分析显示,蛋白泛素化途径在IS中上调,在IR中下调。循环代谢物分析显示IR受试者运动后脂质(酰基肉碱和中长链脂肪酸)和碳水化合物(葡萄糖)升高,IS受试者运动后氨基酸代谢反应强烈导致苹果酸、乳酸、次黄嘌呤/黄嘌呤(ATP转换)和丙氨酸(肌肉氨解毒)积累增多。IR受试者运动后,大多数复杂脂质(51%)出现更强烈地积累,不饱和TAG(4-12个不饱和度)运动后迅速积累,而饱和TAG(0-3个不饱和)在IS中下降更多,表明水解效率更高。同时胃抑制多肽(GIP)、瘦素和胃饥饿素等代谢激素在IS受试者运动后下降更强烈。此外,作者观察到IR受试者能量稳态受损(图6)。
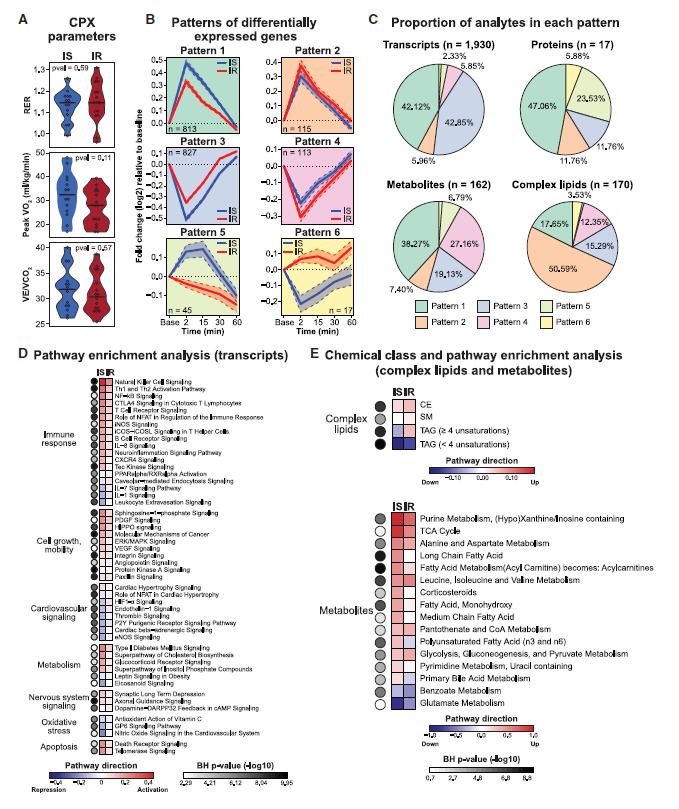
图6 胰岛素抵抗患者对急性运动的不同反应
小结
本研究结合纵向多组学分子谱与密集采样,首次全面地分析了急性运动在分子层面是如何对人体产生影响的,揭示了骨骼肌、脂肪组织、免疫细胞、肝脏和心血管系统等不同体系之间复杂的相互作用,并筛选出参与运动的重要生物过程潜在调节因子。运动反应受到胰岛素抵抗状态的影响,胰岛素抵抗可调节炎症和心血管反应。本研究虽有研究队列小的局限性,但深度表型分型结合个性化运动测量是迄今为止最全面的分子研究之一,具有发现有氧适应度的静息生物标志物的潜在转化意义,并证明了运动分子测试对阐明胰岛素抵抗机制差异具有关键价值,期望通过血检就可以为运动后发生的分子生理改变提供全景式的分析,对个人健康监测有着重要意义。
参考文献
Contrepois et al., Molecular Choreography of Acute Exercise. Cell 181, 1112–1130, May 28, 2020. https://doi.org/10.1016/j.cell.2020.04.043.
原文阅读,请长按识别下方二维码

精彩推荐
1. Cell Metabolism | 运动调控肠道菌群与代谢物预防糖尿病
2. Nature Medicine | 你离顶级运动员一菌之遥
3. The EMBO Journal | 运动产生的α-KG通过OXGR1刺激肌肉肥厚和脂肪分解



