文献解读
客户案例 | 肺癌中果糖代谢通路的促癌新机制
GLUT5-mediated fructose utilization drives lung cancer growth by stimulating fatty acid synthesis and AMPK/mTORC1 signaling
期刊名:JCI Insight, IF=6.01
研究对象:肺癌
技术平台:XploreMET™ 非靶向代谢组学、同位素示踪技术等
合作单位:上海中医药大学附属龙华医院、上海市中医药研究院中医肿瘤研究所
发表时间:2020.02
肺癌是我国发病率和致死率均排首位的恶性肿瘤,目前认为,代谢重编程是肿瘤的核心恶性特征之一,并且在肿瘤的发生发展过程起重要作用。本研究应用临床大样本、以及各种体外和体内模型深入研究发现,肺癌细胞由于能量代谢极其活跃,故导致肿瘤微环境中能源营养物质不足,此时,肺癌细胞可转向利用血液系统中的第二大血糖——果糖来维持细胞代谢活性,并激活下游的促癌信号通路,从而促进肺癌细胞的恶性生长。
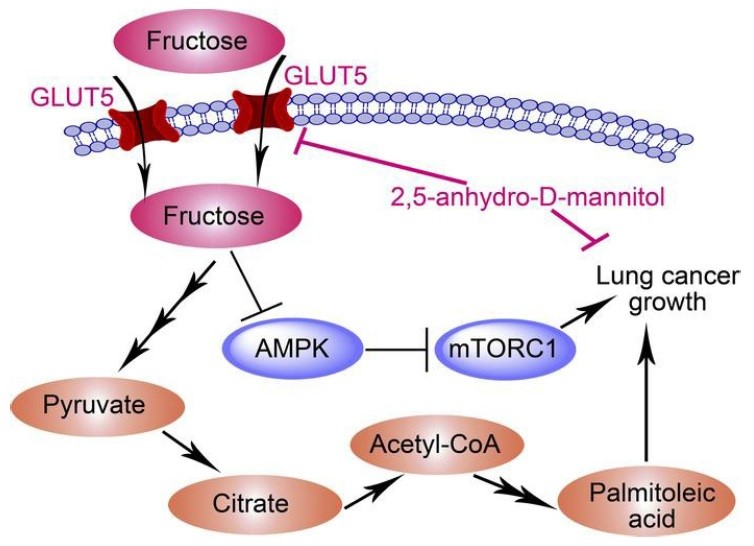
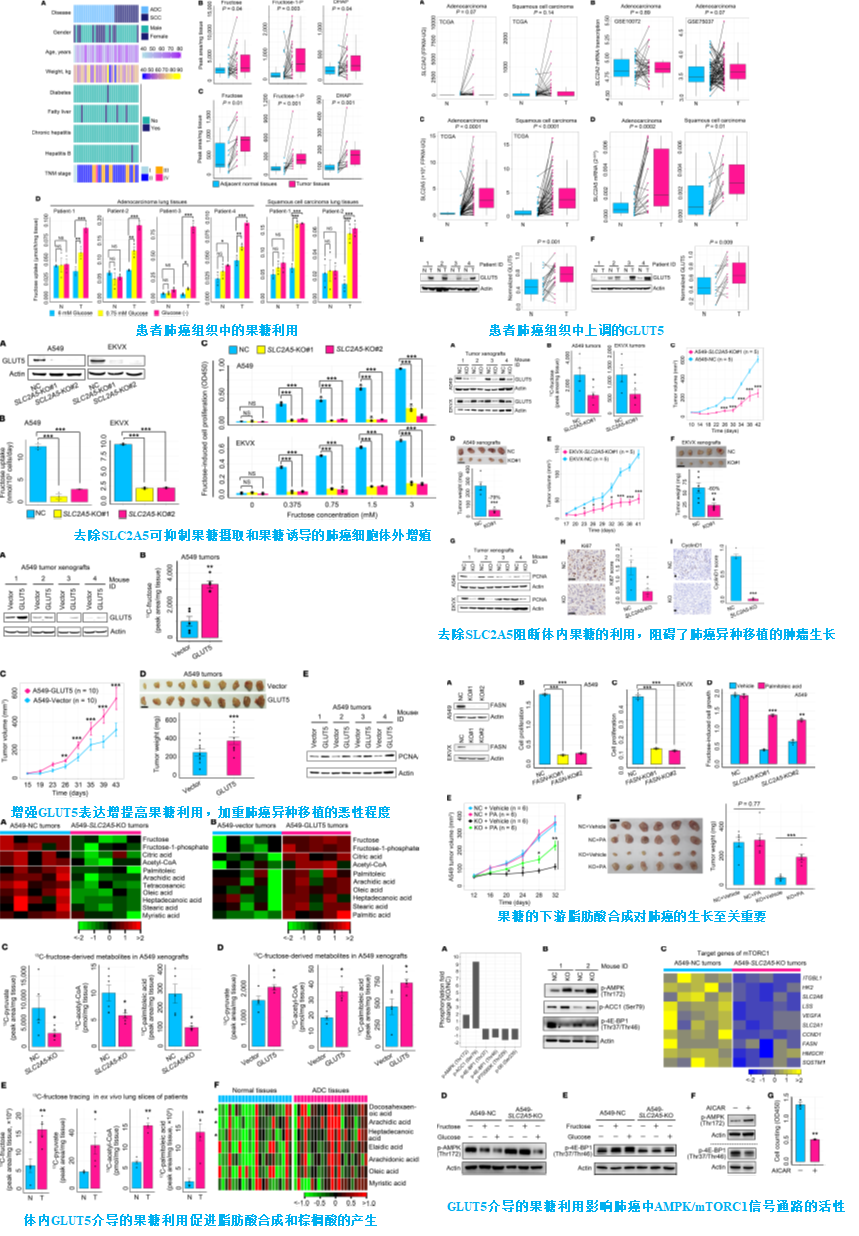
研究人员首先对肺癌患者的组织样本进行代谢组学分析,发现肺癌组织中有高度活跃的果糖代谢活性。在体内代谢养分共存的情况下,肺癌细胞通过上调GLUT5(Glucose transporter 5,由溶质载体家族2成员5(SLC2A5)编码)表达来利用果糖作为葡萄糖替代能源。然后利用同位素标记的代谢物示踪技术,发现果糖分解代谢促进了脂肪酸合成和棕榈油酸的产生,从而加速体内肺癌的恶性生长。而体外和体内补充棕榈油酸均可恢复SLC2A5缺失引起的肺癌增殖受损。此外,分子机制研究表明,GLUT5介导的果糖代谢通路通过抑制AMPK活性,进而激活mTORC1活性促进肺癌细胞生长。GLUT5抑制剂阻断对体内果糖的利用从而显著抑制肺癌生长。
由此证实,体内GLUT5介导的果糖利用在控制肺癌生长中至关重要,靶向果糖转运子GLUT5及果糖代谢通路是肺癌的新型治疗靶点,GLUT5的小分子抑制剂是新型潜在治疗药物,本研究有望从代谢重编程角度为肺癌治疗提供新的策略。
参考文献
Wen-Lian Chen et al. GLUT5-mediated fructose utilization drives lung cancer growth by stimulating fatty acid synthesis and AMPK/mTORC1 signaling. JCI Insight. 2020; 5(3): e131596.
原文阅读,请长按识别下方二维码

精彩推荐
1. Nature Medicine | 肺肿瘤起始细胞依赖蛋氨酸代谢
2. Cell Metabolism | 黑色素瘤和乳腺癌通过上调丝氨酸合成获得生长优势
3.Nature Communications | 受体酪氨酸激酶驱动癌症的代谢弱点



