文献解读
Nature Communications | 饮食限制半胱氨酸和甲硫氨酸使胶质瘤对铁死亡敏感并诱导能量代谢的改变
胶质母细胞瘤(GBM)是最常见的恶性原发性脑肿瘤,目前主要治疗手段是手术治疗,并辅助以放化疗,但总体预后效果较差,长期生存率很低,且GBM治疗耐药性与氧化应激以及谷胱甘肽代谢有关。谷胱甘肽是通过谷胱甘肽过氧化物酶4(GPX-4)活性来抑制脂质过氧化的关键细胞抗氧化剂,它直接由含硫氨基酸半胱氨酸产生,并通过转硫途径间接由甲硫氨酸产生。铁死亡是一种铁依赖性的和由脂质过氧化介导的受调节的细胞死亡形式,前期研究发现包括GBM在内的许多癌细胞系对铁死亡诱导剂都很敏感,且半胱氨酸剥夺的药理学方法已被证明对其他癌症有效。

2023年3月2日,哥伦比亚大学医学中心的研究团队在Nature Communications(IF 17.694)期刊上发表题为“Dietary restriction of cysteine and methionine sensitizes gliomas to ferroptosis and induces alterations in energetic metabolism”的研究型文章,本研究表明,在小鼠和人胶质瘤细胞系以及体外器官型切片培养中,半胱氨酸和甲硫氨酸剥夺(CMD)饮食可以与GPX4抑制剂RSL3协同作用,增加细胞铁死亡和脂质过氧化。在同基因原位胶质瘤小鼠模型中,半胱氨酸缺失和甲硫氨酸限制饮食可以改善对RSL3的治疗反应并延长生存期。CMD饮食导致体内代谢组学、蛋白质组学和脂质组学的明显改变,这突出了通过非侵入性饮食改变来提高胶质瘤治疗中铁死亡疗效的潜力。
技术路线图
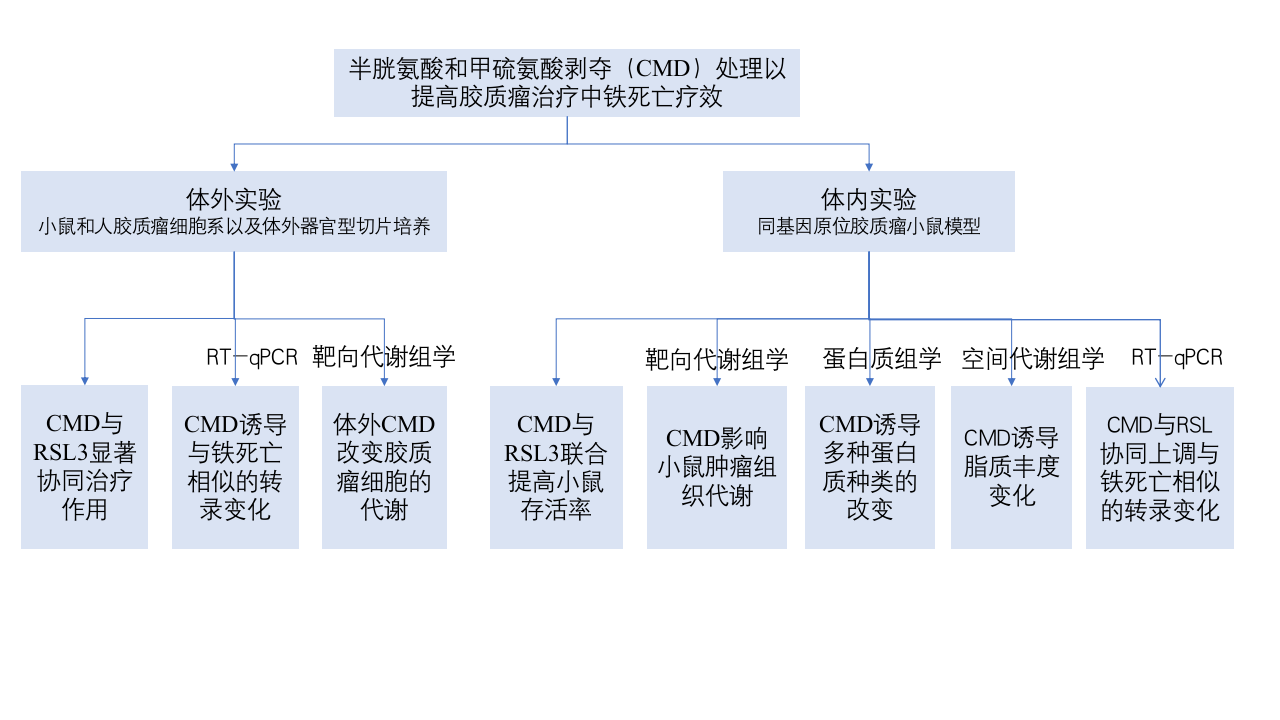
CMD使胶质瘤细胞对RSL3诱导的铁死亡敏感
以小鼠和人胶质瘤细胞系以及体外器官型切片培养为实验材料,通过细胞培养、活细胞共聚焦显微镜以及流式细胞术等方法发现,从培养基中去除半胱氨酸和甲硫氨酸(CMD)与RSL3介导胶质瘤细胞的铁死亡具有显著的协同作用,并且低剂量(100 nM)RSL3联合CMD可以将脂质过氧化作用增加到相当于高剂量(500 nM)RSL3的水平。
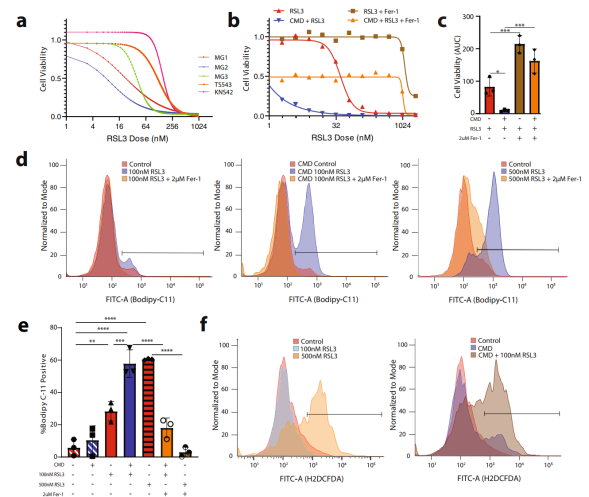
图1. CMD使胶质瘤细胞对RSL3诱导的铁死亡敏感
CMD诱导的转录变化通常与铁死亡相关
以小鼠和人胶质瘤细胞系以及体外器官型切片培养为实验材料,通过实时荧光定量PCR(RT-qPCR)发现,CMD会诱导与铁死亡相似的转录变化,包括CHAC1、PTGS、SLC7a11和ATF4 mRNAs水平上调。
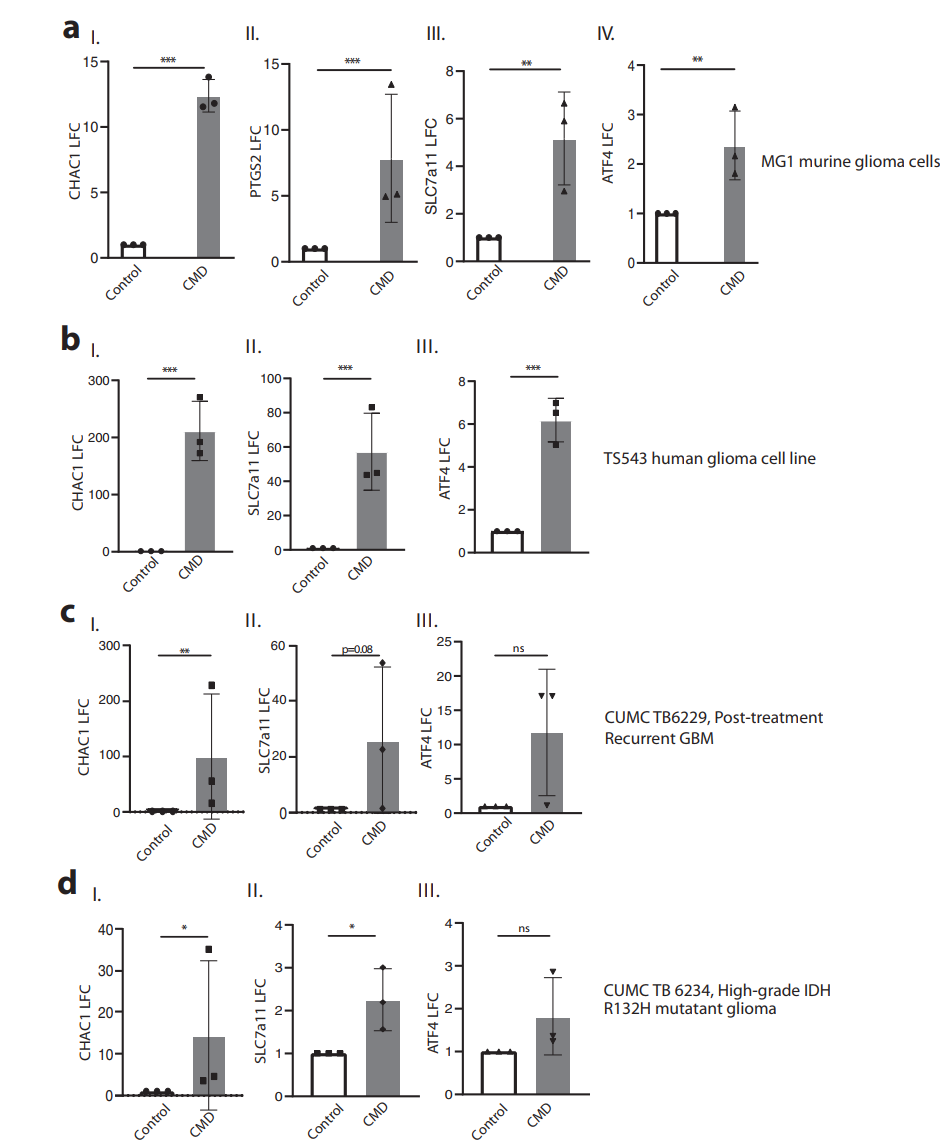
图2. CMD诱导与铁死亡相关的转录特征
CMD会改变胶质瘤细胞的代谢
以两种小鼠胶质瘤细胞系(MG1和MG3)为实验材料,首先过对100多种代谢物进行靶向代谢物检测,发现CMD处理显著影响了半胱氨酸/甲硫氨酸代谢、甘氨酸-脯氨酸代谢、牛磺酸/次牛磺酸代谢、丙氨酸/天冬氨酸/谷氨酸代谢以及硒复合代谢,并进一步使用与半胱氨酸/甲硫氨酸代谢相关23种内标物的靶向代谢物检测发现CMD处理使胶质瘤细胞的氧化型和还原型谷胱甘肽、谷氨酸和次牛磺酸/牛磺酸显著减少。
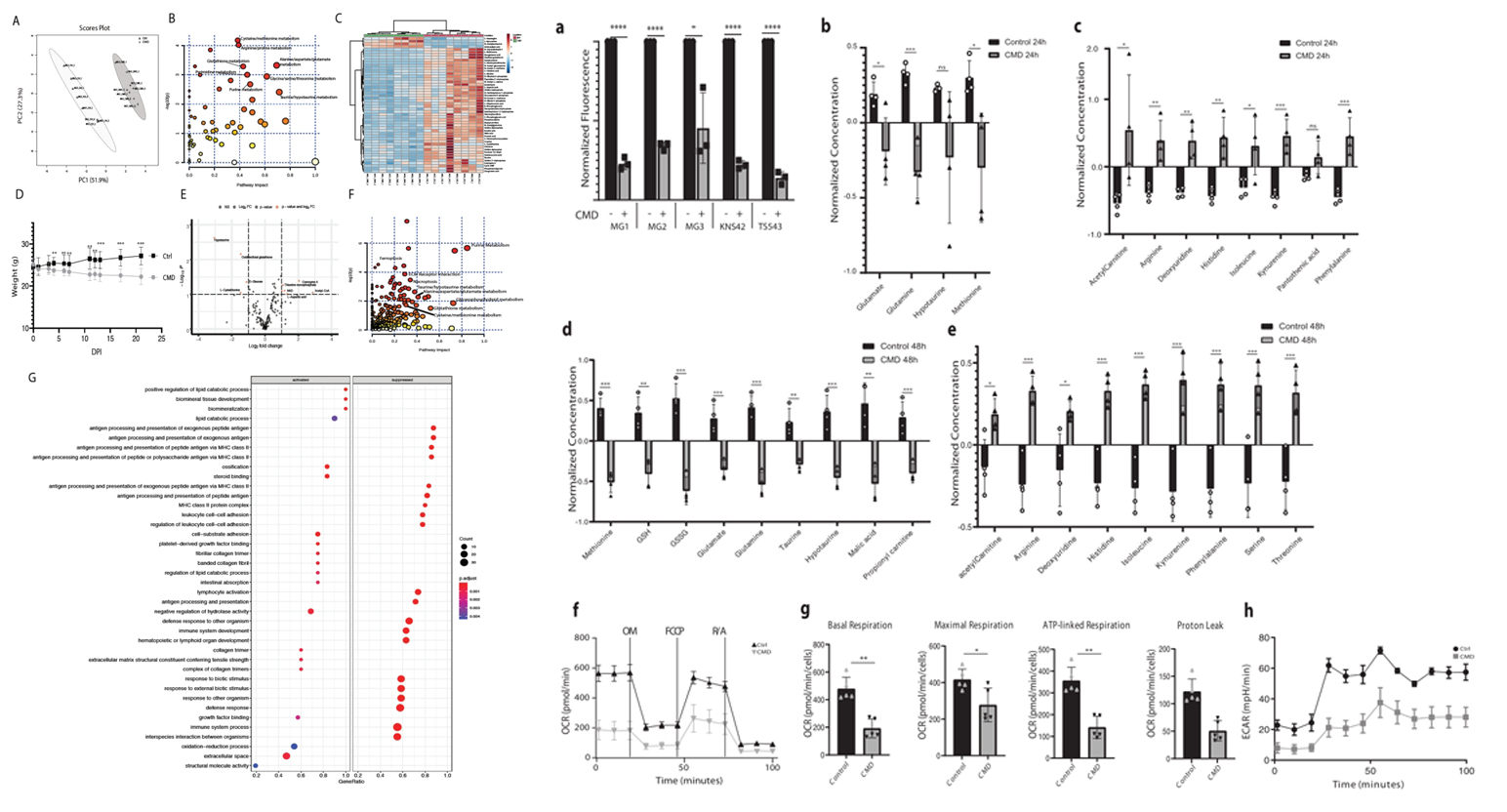
图3. CMD改变胶质瘤细胞的代谢
CMD可提高胶质瘤小鼠存活率,并且诱导小鼠体内脂质组、代谢组和蛋白质组的变化
以同基因原位胶质瘤小鼠模型为实验材料,通过Kaplan-Meier生存分析显示,尽管CMD饮食小鼠体重较轻,但CMD饮食小鼠的生存优势明显高于对照组荷瘤小鼠,并且RSL3和CMD联合治疗的小鼠存活时间明显长于对照组。
通过靶向代谢组学方法,发现CMD处理小鼠肿瘤组织中多种代谢物浓度降低(包括乙酰蛋氨酸、腺苷基同型半胱氨酸、半胱氨酸、氧化谷胱甘肽和甲硫氨酸等),并且牛磺酸/次牛磺酸代谢、谷胱甘肽代谢、精氨酸代谢、TCA循环和脂肪酸延伸/降解等代谢通路发生了关键变化。通过蛋白质组学分析,CMD诱导了多种蛋白质改变,其中最显著富集通路是脂质分解代谢通路,并且CMD导致了一个强烈的免疫抑制特征,包括与抗原呈递和淋巴细胞活化相关的蛋白下调。蛋白质组学和代谢组学的联合分析显示,半胱氨酸/甲硫氨酸代谢、谷胱甘肽代谢、铁死亡、甘油磷脂代谢等相关途径显著改变。使用解吸电喷雾成像质谱(DESI-IMS)进行空间代谢组学分析,观察到CMD小鼠胶质瘤组织中更显著的脂质丰度变化,包括FA 18:2、FA 18:1、PS 18:22:6、PI 18:0_20:4等脂质相对丰度显著增加,以及PC 16:0_18:1、PE 18:0_20:4、PC 16:0_20:4、PE 16:0_22:6和腺苷酸的相对丰度显著减少。通过RT-qPCR检测发现CMD和RSL3协同作用显著上调了体内与铁死亡相关的转录本。
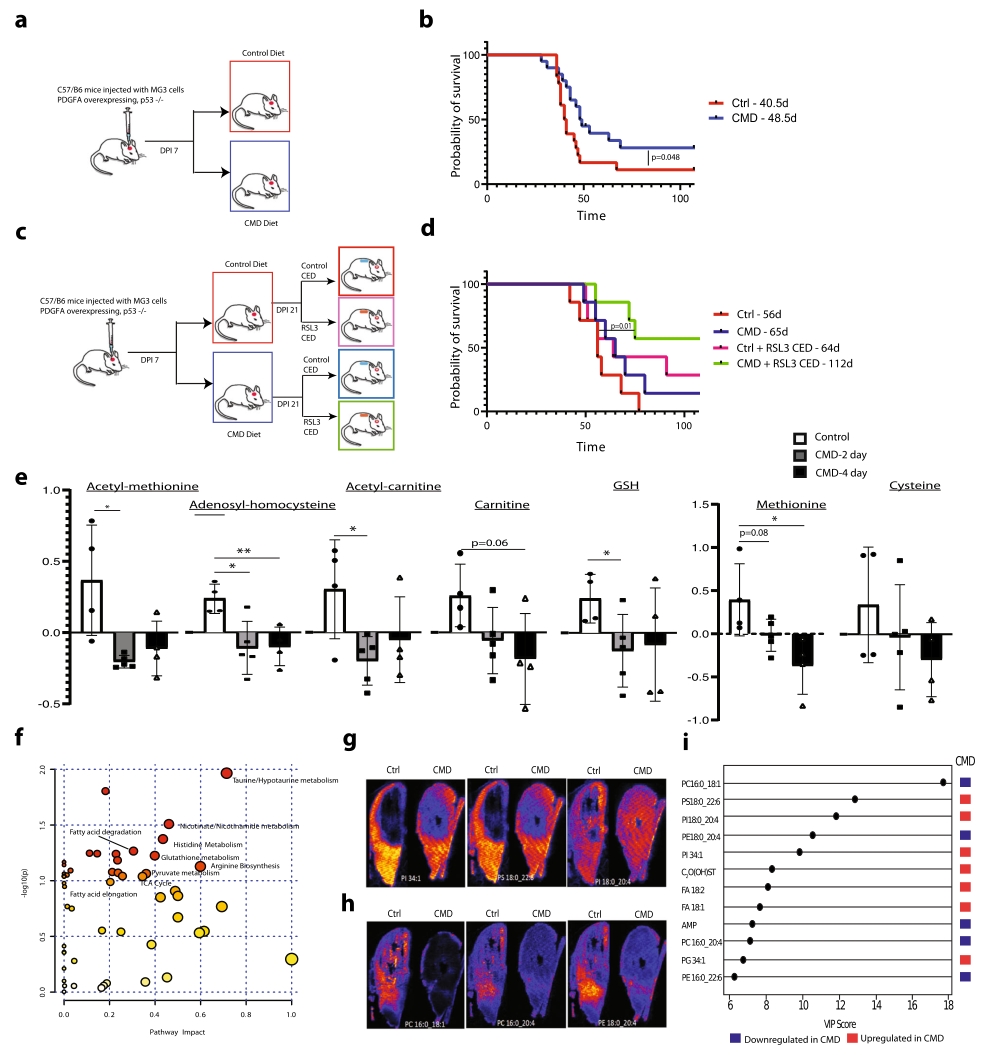
图4. CMD提高胶质瘤小鼠生存率与小鼠体内代谢组学、蛋白质组学和脂质组学改变有关
小结
铁死亡是一种很有前途的癌症治疗方法,这种新型的程序性细胞死亡是由抑制GPX4诱导的,GPX4可以利用谷胱甘肽解毒脂质过氧化物来抑制铁死亡。本研究发现小鼠和人胶质瘤细胞通过RSL3等药物抑制GPX4而容易发生铁死亡,并且RSL3介导的细胞死亡是铁死亡特异性的(独立于细胞凋亡或坏死死亡),与脂质过氧化增加有关。同时也证明了CMD会降低肿瘤细胞存活率,并且与RSL3协同增加脂质过氧化和细胞死亡。人胶质瘤离体切片表现出对CMD和铁死亡诱导剂的协同作用敏感性体内CMD饮食导致肿瘤的脂质组学、蛋白质组学和代谢组学特征发生显著变化,生存率有所提高。与对照相比,CMD饮食和局部递送RSL3联合治疗可显著提高生存率。
参考文献
Upadhyayula PS et al. Dietary restriction of cysteine and methionine sensitizes gliomas to ferroptosis and induces alterations in energetic metabolism. Nat Commun. 2023.
请扫描二维码阅读原文

绘谱帮你测
麦特绘谱开创性地搭建了医学领域高端代谢组学技术平台,覆盖了非靶向-全定量-代谢流等全方位的高端医学代谢组解决方案,同时全面布局微生物组学、转录组学和蛋白质组学等多组学技术服务,已成为全球多组学研究者的优选合作伙伴。麦特绘谱拥有Q1000,Q500、Q300、Q200和胆汁酸、短链脂肪酸、色氨酸及吲哚衍生物、多胺和TMAO类等各类小分子代谢物、非靶向代谢组学和同位素示踪代谢流技术等共40+系列检测方法;已为数百家三甲医院、科研院所和企业提供多组学解决方案,协助客户与合作伙伴发表SCI文章300+篇,累计影响因子3000+,平均IF> 10,包括Science, Nature, Cell Metabolism,Immunity, Gut, Hepatology, Microbiome等顶级期刊。


