文献解读
Cell Metabolism | 靶向肝脏GLS1可改善非酒精性脂肪肝
非酒精性脂肪肝(NAFLD)是一种广受关注的全球性疾病,其特征为代谢重编程导致的肝脏脂肪累积,包括脂肪酸摄取量增加、线粒体脂肪酸β氧化(FAO)降低、脂肪酸从头合成脂肪增加,以及极低密度脂蛋白(VLDL)的组装和分泌功能失调等。另一方面,非酒精性脂肪性肝炎(NASH)是一种更具侵袭性的形式,其特征是肝细胞坏死性炎症和纤维化,是肝硬化和肝癌的重要危险因素。VLDL合成和分泌功能失调是NASH的主要特征。
谷氨酰胺酶是肝脏谷氨酰胺代谢的主要调节酶,且其中谷氨酰胺酶1(GLS1)已被证明可以抑制肝纤维化的进展,但是GLS1与NAFLD相关性尚缺乏深入研究。本文作者通过研究表明,GLS1在NASH的状态下会过表达,且对于GLS1特定的抑制作用可减轻肝脏脂肪变性和氧化应激,因此GLS1可作为一个潜在的NASH治疗靶点,相关成果发表在《Cell Metabolism》上。
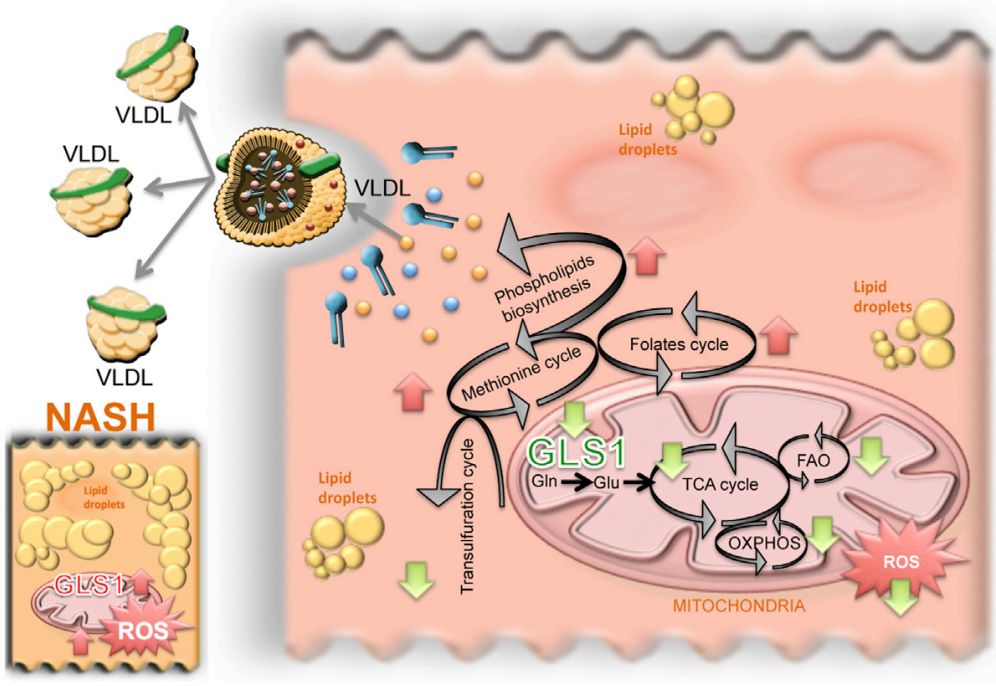
谷氨酰胺酶1(GLS1)在NASH临床患者和小鼠中都过表达
对一大型队列(健康对照和NASH患者)进行血清谷氨酰胺和谷氨酸(谷氨酰胺酶反应产物)水平检测,结果显示两组中谷氨酰胺虽无明显差异,但NASH患者的血清中谷氨酸显著升高(图1A),表明NASH患者的谷氨酰胺分解代谢是异常的。同样地,在另一个队列中,NASH患者GLS1的mRNA水平比健康者高。此外,通常在健康肝静脉周围肝细胞中表达的谷氨酰胺合成酶被诱导,催化谷氨酸合成谷氨酰胺并消除门静脉周肝细胞解毒的残留氨(图1B, 1C)。

Figure 1. 谷氨酰胺酶1(GLS1)在临床非酒精性脂肪性肝炎中过表达
进一步评估NASH临床前小鼠模型(胆碱和蛋氨酸缺乏饮食MCDD)的GLS1表达水平,结果显示GLS1的蛋白和mRNA水平以时间依赖性升高(图2A-2C)。0.1% MCDD(胆碱缺乏和0.1%蛋氨酸饮食)饮食四周后,GLS1主要累积在肝细胞中(图2E)。

Figure 2. 谷氨酰胺酶1(GLS1)在胆碱和蛋氨酸剥夺而诱导NASH小鼠模型中过表达
体外/体内靶向GLS1可改善肝脏脂肪变性
为了鉴定因胆碱和蛋氨酸剥夺而诱导NASH小鼠模型中GLS1表达的主要肝细胞,研究人员将小鼠肝脏分离肝细胞和肝基质细胞。结果显示,0.1% MCDD后分离的肝细胞中Gls1的mRNA水平显著升高。同样地,体外激活的培养小鼠原代HSC中,7天后Gls1 mRNA水平增加,与增加的HSC活化对应。利用MCD培养原代肝细胞48 h,沉默Gls1降低了甘油三酯的积累(图3A-3C),去分化参数,比如白蛋白、胎蛋白和HNF4,在mRNA水平上均未改变。因此,沉默GLS1可减轻分离的肝细胞脂肪变性。
随后,对0.1% MCDD小鼠进行Gls1沉默处理,肝脏GLS1水平降低,GLS2表达增加,谷氨酰胺合成酶表达在蛋白质水平上没有明显改变。在这种情况下,通过测定13C标记的谷氨酰胺到谷氨酸确定谷氨酰胺酶活性降低,证实了一方面谷氨酰胺酶活性在饮食中被诱导,另一方面在体内Gls1沉默后谷氨酰胺酶活性下降的趋势。重要的是,在mRNA和蛋白水平上,体内GLS1特异性沉默显著减轻了肝脏脂肪变性(图3D)。

Figure 3. 体外和体内靶向沉默谷氨酰胺酶1(GLS1)缓解肝甘油三酯和非酒精性脂肪性肝炎的积聚
蛋氨酸和胆碱剥夺后体内外靶向GLS1可恢复VLDL的分泌
磷脂需要VLDL的正确组装,蛋氨酸和胆碱的剥夺会导致VLDL的分泌受损。研究人员评估了体内外Ptd-Chol合成和VLDL分泌中Gls1沉默的作用。利用(U-13C)葡萄糖培养和质谱分析,发现在蛋氨酸和胆碱剥夺的情况下,Ptd-Chol中碳示踪剂呈降低趋势,反映了葡萄糖合成Ptd-Chol受损,而Gls1沉默促进了一些Ptd-Chol的合成。此外,利用lomitapide(可阻碍VLDL分泌)处理分离的小鼠肝细胞,结果发现细胞脂质积累的程度与蛋氨酸和胆碱剥夺类似。有趣的是,在这些条件下,Gls1沉默不能阻止lomitapide处理后细胞脂质的积累,提示Gls1沉默诱导的降脂可能与VLDL的分泌有关。
此外,0.1% MCDD体内沉默Gls1后,肝脏Ptd-Chol和磷酯酰丝氨酸(Ptd-Ser)水平升高,而Ptd-Et的水平不变(图4B);分泌的VLDL颗粒的脂质成分如甘油三酯、磷脂和胆固醇衍生物显著增加(图4C)。因此,Gls1沉默通过靶向VLDL组装来减轻肝脏脂肪变性。
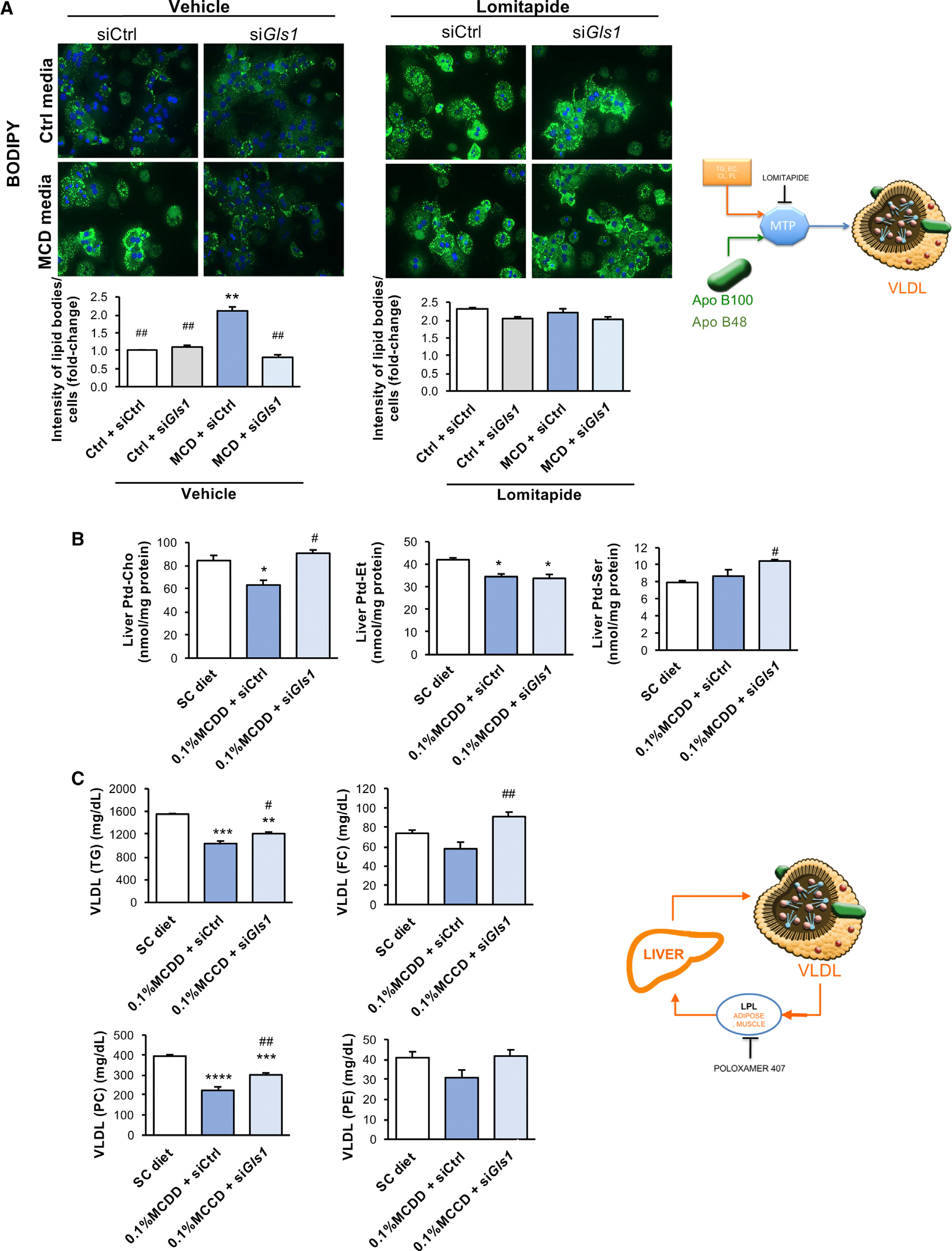
Figure 4. 体外和体内靶向谷氨酰胺酶1(GLS1)恢复胆碱和蛋氨酸剥夺后极低密度脂蛋白(VLDL)甘油三酯的输出
体内外靶向GLS1降低氧化应激
氧化应激在NASH的发病机理和进程中起着至关重要的作用。研究发现,蛋氨酸和胆碱缺乏培养的小鼠原代肝细胞中总的和线粒体活性氧(ROS)水平是升高的(图5A)。四周0.1% MCDD与氧化型谷胱甘肽(GSSG)/还原型谷胱甘肽(GSH)比例和标记的谷氨酰胺到GSH的增加有关。在这些条件下GSH合成增加,并在Gls1沉默下恢复(图5B)。CD-HFD饮食小鼠在GLS1沉默条件下,GSSG/GSH也降低(图5C),脂质过氧化标志物丙二醛(MDA)水平降低(图5D)。值得注意的是,Gls1沉默可显著降低原代肝细胞和体内NASH模型中的氧化应激。
接下来,研究人员通过U-13C谷氨酰胺到1-13C柠檬酸测定了肝脏TCA循环活性,通过放射性标记的棕榈酸到CO2和氧化型酸-溶解代谢物(ASM)测定肝脏FAO,以及通过耗氧率测定线粒体氧化磷酸化(OXPHOS)。四周0.1% MCDD后,所有分析参数明显升高,重要的是,Gls1沉默可恢复TCA、β氧化和OXPHOS通量,以控制与氧化应激降低的饮食水平(图5E-5G)。因此,体内外靶向GLS1可通过减少氧化代谢来降低ROS水平。
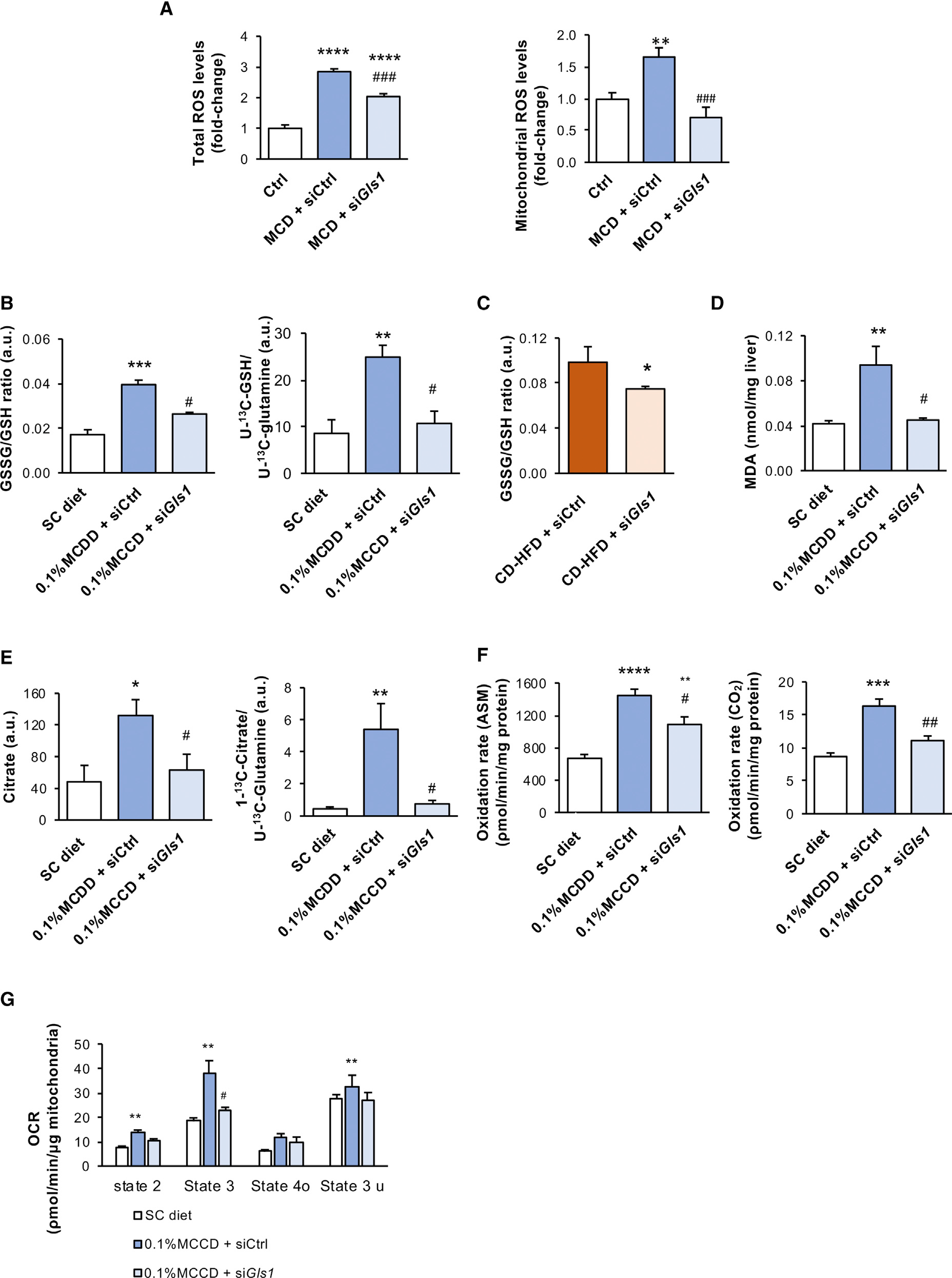
Figure 5. 体内外靶向谷氨酰胺酶1(GLS1)降低氧化应激
GLS1介导的氧化应激与肝脏磷脂含量的恢复有关
Gls1沉默后,参与转硫途径的基因表达降低,而参与叶酸和蛋氨酸循环的酶的表达增加(图6A)。同样地,Gls1沉默可诱导参与CDP-胆碱和CDP-乙醇胺途径的基因mRNA水平和催化不同磷脂之间碱基交换的酶(图6B)。

Figure 6. GLS1介导的氧化应激的减少与磷脂合成增加以及叶酸和蛋氨酸循环的激活有关
小结
本文通过GLS1基因沉默以及脂质组和13C代谢流分析等技术,发现抑制GLS1促进了丝氨酸代谢重编程,从谷胱甘肽生成和一碳代谢循环转移到蛋氨酸循环,恢复了肝脏磷脂酰胆碱(PC)含量和极低密度脂蛋白的分泌,有效缓解脂肪变性,验证了GLS1相关的脂代谢在NASH的氧化还原和肝脏脂肪积累中至关重要的作用。该研究表明靶向作用GLS1是一种有价值的治疗NASH的方法。
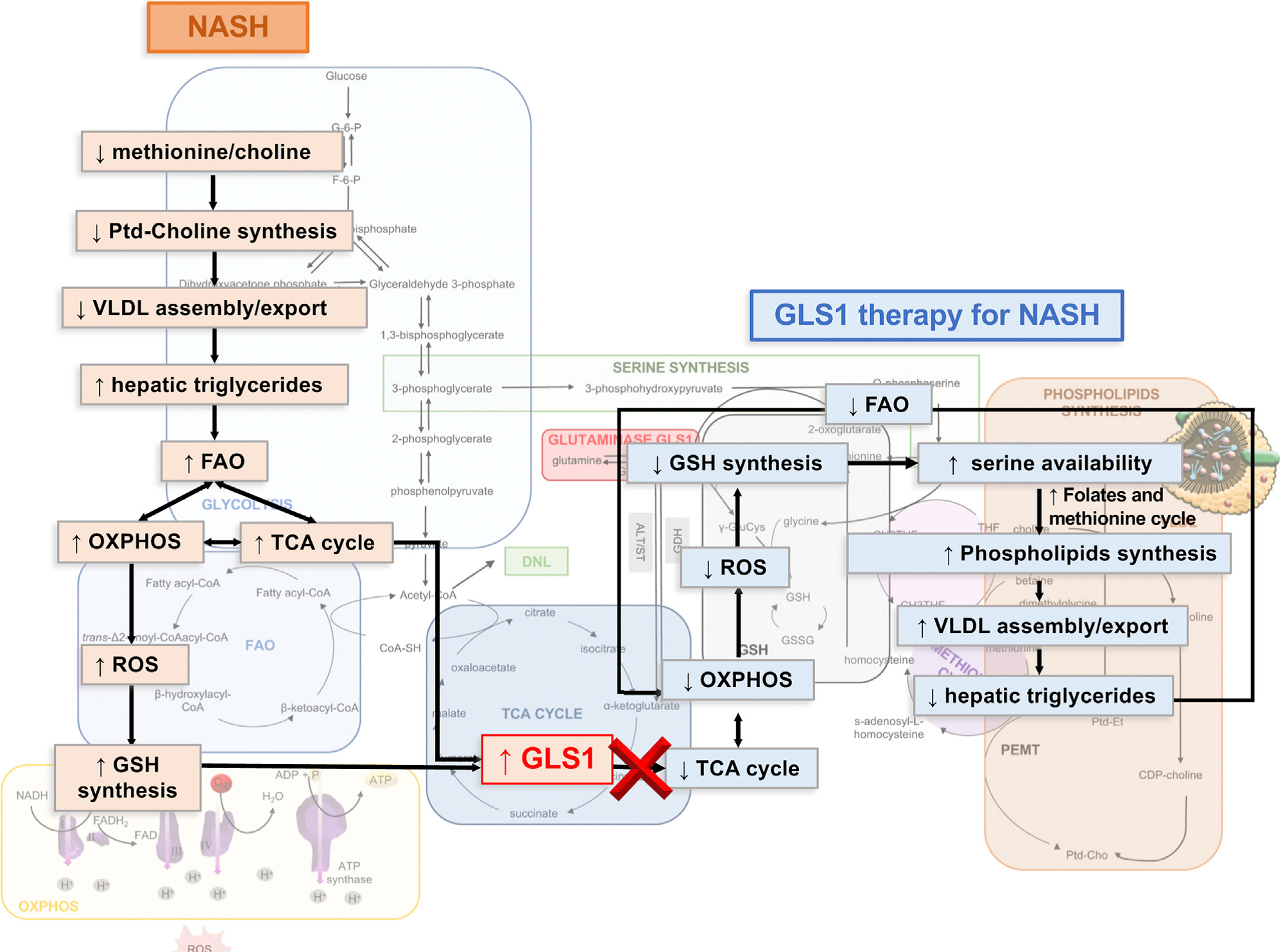
Figure 7. 谷氨酰胺酶1(GLS1)抑制非酒精性脂肪性肝炎的流程图
上述研究中涉及到的脂质组和代谢流技术
麦特绘谱均可提供检测与分析服务
以及代谢组学全套解决方案
欢迎各位老师来“撩”~
参考文献
Targeting Hepatic Glutaminase 1 Ameliorates Nonalcoholic Steatohepatitis by Restoring Very-Low-Density Lipoprotein Triglyceride Assembly. Cell Metabolism. 2020.
原文阅读,请长按识别下方二维码

精彩推荐
2. Nature Communications | 谷氨酰胺氮代谢转变有助于癌症恶性进展
3. Gut | 菌群色氨酸代谢激活芳烃受体并改善酒精性肝损伤
4.『珍藏版』Cell Metab综述 | 非酒精性脂肪肝基于肠道微生物组的个性化医疗的最新概念,机遇和挑战
5. 客户案例|一种新型ASBT抑制剂 – IMB17-15可抑制非酒精性脂肪肝进展
8. Nature Medicine: 浅析NAFLD/NASH模型,助您科研无忧!



