文献解读
Trends in Immunology | 多胺和犬尿氨酸的免疫调节
多胺(即腐胺、亚精胺和精胺)是具有生物活性的多聚阳离子,能够结合核酸和蛋白质并调节信号传导途径。多胺功能已经在肿瘤中得到广泛的研究,它们可以促进细胞转化和增殖。研究发现亚精胺通过吲哚胺2,3-双加氧酶1(IDO1)在多发性硬化(MS)的实验模型中发挥保护作用,并赋予树突状细胞(DCs)免疫调节特性。IDO1将L-色氨酸(Trp)转化为犬尿氨酸(Kyn),并通过激活芳香烃受体(AhR)发挥多种免疫调节作用。AhR激活增加了多胺的产生,因此多胺和犬尿氨酸是免疫调节回路的参与者,对自身免疫性疾病和癌症的免疫治疗具有潜在影响。相关成果发表在《Trends in Immunology》。

多胺的生物合成和代谢
多胺生物合成的第一步-鸟氨酸(Orn,精氨酸(Arg)由精氨酸酶1(ARG1)代谢生成)脱羧生成(图1)。限速酶鸟氨酸脱羧酶1(ODC1)催化Orn转化为腐胺,ODC1是一种依赖磷酸吡哆醛(PLP)限速酶,其表达是在响应多种刺激(如激素、癌基因、生长因子和多胺本身)的反应中被诱导。ODC1活性受转录、翻译和翻译后水平控制,实际上,ODC1受到泛素非依赖蛋白酶体降解机制的影响,该机制涉及到抗酶1(AZ1)和ODC抗酶抑制剂(AZIN1)蛋白。多胺生物合成的下一步是由亚精胺合酶(SPDS)催化,产生亚精胺,再由由精胺合酶(SPMS)转化为精胺(图1)。
在过去几十年里,多胺的分解代谢(包括高级多胺反转化为腐胺)变得越来越重要,因为它极大地影响细胞内每种多胺的总量。精胺和亚精胺通过两个连续反应分别转化为亚精胺或腐胺,即亚精胺/精胺N-1-乙酰转移酶(SSAT)催化的乙酰化反应和乙酰多胺氧化酶(APAO)介导的氧化反应(图1)。多胺可在多个水平调节SSAT活性,包括转录、mRNA处理、mRNA翻译和蛋白质降解。此外,SSAT的表达可由多种刺激因子诱导,包括毒素、激素、细胞因子、白藜芦醇等天然产物、应激途径和大鼠缺血再灌注损伤。与SSAT相比,APAO在人体正常组织中均有表达,其活性受到SSAT生成的乙酰化中间产物可用性的限制。此外,精胺可通过精胺氧化酶(SMOX)催化直接氧化为亚精胺(图1)。鉴于多胺可通过APAO和SMOX氧化酶分解代谢产生有毒的ROS,因此必须对多胺代谢进行精细调节,这不仅是为了平衡多胺的含量,而且也是为了防止细胞氧化应激和损伤。
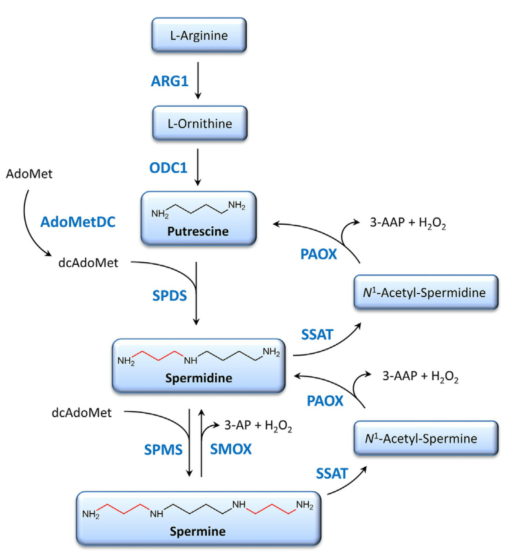
图1 哺乳动物多胺的代谢
由于其阳离子性质,多胺需要跨膜转运。溶质载体家族(SLC)、有机阳离子转运体(OCT)和阳离子氨基酸转运体(CAT)是决定多胺通量的主要载体。SLC家族成员还可以通过将腐胺和乙酰化亚精胺与细胞外Arg交换来供给多胺分泌。SLC的一个特殊亚型SLC18B1介导了胚胎大鼠星形胶质细胞和小鼠骨髓源性肥大细胞中精胺和亚精胺的囊泡储存和随后的胞吐,分别参与神经传递和免疫细胞脱颗粒。多胺摄取也可以增加对增殖刺激的反应。为了确保多胺稳态,这些转运蛋白的活性受AZ1和AZIN1的调控,AZ1和AZIN1分别抑制和增强哺乳动物细胞对胞外多胺的吸收。除了可饱和转运蛋白外,多胺还可以通过网格蛋白(或磷脂酰肌醇蛋白聚糖)1依赖性内吞作用被吸收,不过此调节机制尚未被阐明。
多胺的免疫调节
通过减少半必需氨基酸Arg的可用性,ARG1可直接控制T细胞增殖和分化。髓样来源的抑制细胞(MDSC)、巨噬细胞和DCs可代谢局部Arg,导致Arg局部饥饿,通过损害T细胞受体(TCR)CD3-ξ链在人和小鼠细胞中的表达,从而阻断T细胞G0-G1周期的进展。此外,精氨酸代谢可产生具有多种免疫调节特性的多胺。一方面,多胺对小鼠CD4+和CD8+T淋巴细胞的活化和增殖是必需的,另一方面,它们在免疫细胞中发挥不同的作用,影响着T细胞的命运和适应性(图2)。
此外,在干扰素(IFN)-γ和Toll样受体(TLR7)刺激驱动的炎症条件下,DCs中的亚精胺含量降低,同时细胞代谢平衡从线粒体氧化磷酸化(OXPHOS)向糖酵解倾斜。此外,亚精胺激活FOXO3通路,抑制炎性肿瘤坏死因子(TNF)-α和白细胞介素(IL)-6细胞因子的产生,并可通过吲哚胺2,3-双加氧酶1 (IDO1)的Src激酶依赖性磷酸化,将小鼠DCs重编为免疫调节表型。反过来,代谢中间体又介导非经典NF-κB途径的激活,并诱导IDO1自身和免疫抑制性转化生长因子β1(TGF-β1)的表达。
与DCs不同,通过亚精胺依赖性的OXPHOS代谢诱导,小鼠骨髓衍生的巨噬细胞可进行ARG1表达的替代激活和抑制促炎细胞因子表达。据报道,这种协同作用可减少自身免疫性CD4+和CD8+T淋巴细胞浸润中枢神经系统,并降低实验性自身免疫性脑脊髓炎的临床评分。除了上述免疫调节特性外,研究人员基于自身免疫表观遗传调控证据还提出了另一种“多胺假说”。通过与S-腺苷甲硫氨酸竞争以用于自身合成,多胺可干扰组蛋白甲基化,从而改变正常基因表达。由此产生的低甲基化使得先前被掩盖的基因异常表达,因此,可能出现新的自身抗原(如人SLE中的Ro60)。
在肿瘤微环境中,肿瘤细胞和髓系细胞对Arg的分解代谢可抑制细胞毒性CD8+T细胞的功能,使小鼠B16黑色素瘤模型逃避免疫监视。此外,多胺可以加速肿瘤的生长和进展,还可以通过自噬提高抗肿瘤免疫能力。总之,在健康和病理条件下,多胺诱导的免疫结果取决于多种机制的复杂整合。
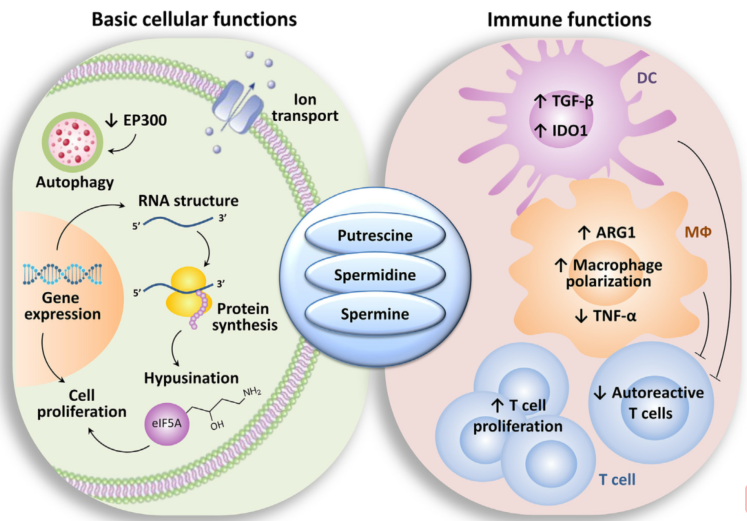
图2 多胺的免疫和非免疫功能
犬尿氨酸生物合成
犬尿氨酸途径(KP)是一系列的酶促反应,第一步和限速步骤由三种不同的酶催化,即色氨酸2,3-双加氧酶(TDO),IDO1及其旁系同源物IDO2(图3)。这三种酶都含有血红素作为辅基,它们使用O2催化Trp吲哚核吡咯环的氧化裂解,形成N-甲酰基犬尿氨酸,进而被芳基甲酰胺酶快速代谢为L-犬尿氨酸。
Kyn是用于NAD+产生途径的主要分支的起源,也是其他侧分支的起源,在该分支中,Kyn被三种氨基转移酶(KAT)转化为犬尿酸(KYNA)。完整的KP(即有两个分支)很少存在于单个细胞中,而是被隔离开来。在主要途径中,Kyn受到几种酶的连续作用,最终形成NAD+(图3)。在哺乳动物中,循环Kyn通过大型氨基酸转运蛋白LAT1很容易穿过血脑屏障,然后被胶质细胞吸收,转化为KYNA或3-HK、3-HAA和QA。此外,在外围环境中,如果微环境中存在IFN-γ,则小鼠IDO1–DCs摄取Kyn并将其转化为犬尿氨酸。因此,Kyn前体存在的情况下,即使不表达TDO或IDO1的细胞中也会产生Kyn。
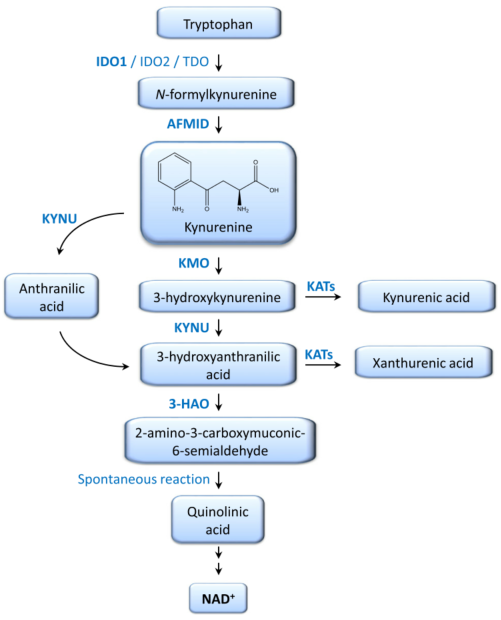
图3 哺乳动物的犬尿氨酸途径
犬尿氨酸的免疫调节
在免疫调节中,Kyn协同机制合作被Trp饥饿所激活。通过剥夺细胞微环境中Trp,IDO1介导了GCN2激酶的应激反应途径激活,该激酶可以减少蛋白质合成并暂时阻断小鼠CD8+T淋巴细胞功能。在同一物种中,低浓度Trp、Kyn和其他Kyn协同促进TCR ζ链的下调和效应CD4+T淋巴细胞向抑制性Foxp3+Treg细胞的转化。
在小鼠中,Kyn还可以通过激活AhR来促进免疫调节作用,在伯氏疟原虫诱导的全身性炎症模型中可诱导血管舒张,这可能是下游代谢产物黄尿酸通过一氧化氮诱导直接引起的,这一点从肠系膜动脉血管反应性研究中得到证实。此外,KYNA可激活GPR35受体促进人单核细胞外渗。3-HAA虽然不是AhR直接激动剂,但研究显示其与核辅激活因子7相互租用并间接增强树突状细胞中AhR激活。
AhR最初被发现是一种具有解毒功能并可被环境污染物激活的受体,后来被界定AhR是一种对外源和内源性分子反应的适应性和先天免疫反应的调节剂。根据配体和组织微环境不同,免疫细胞中AhR激活会产生不同的结果,但Kyn似乎可以在DCs和CD4 + T淋巴细胞中均可促进驱动AhR介导的免疫调节作用。
Kyn和其他吲哚衍生物(并非总是由哺乳动物产生)的重要来源是胃肠道(GI)中的菌群。肠道菌群可以直接吸收Trp,从而限制其宿主的可利用率,并产生激活宿主AhR的Trp代谢产物,其中一些对炎症性肠病具有保护作用。此外,由肠道共生梭状芽孢杆菌产的吲哚3-丙酸可激活孕烷X受体(PXR),在药物诱导的肠道损伤小鼠模型中改善粘膜稳态和屏障功能。
多胺、犬尿氨酸和AhR:免疫和癌症中的功能回路
一些癌症类型(如结肠癌)通过利用多胺代谢失调来促进其增殖。事实上,癌细胞可以从细胞外环境中吸收大量的多胺来促进其生长,从而降低抗肿瘤免疫能力。尽管从概念上讲,抑制多胺利用可用于癌症治疗,但在临床环境中成功应用还很遥远。事实上,基于对多胺代谢关键酶之一的特异性抑制的治疗策略已经失败,主要是由于补偿机制的存在,当单一酶作为靶向目标时,补偿机制可以缓冲这些影响。
最近在一项多发性骨髓瘤(MM)研究中报道了一种有效阻断肿瘤多胺效应的新策略。在人类MM细胞,AhR通过ODC1和AZIN1的直接转录而被激活从而正向调控细胞内多胺产生。据报道,在人类MM细胞中,AhR的表达与存活率呈负相关,这表明AhR抑制有利于MM的治疗。AhR激活还可以上调大鼠肝祖细胞中编码SPDS的基因和人HepG2细胞中编码SMOX的基因,从而进一步促进亚精胺/ AhR反馈环。此外,由于Kyn是AhR的主要内源性激动剂,多胺可增加Kyn的产生,这些数据表明存在一个原促癌和免疫抑制的机制回路,因此推测,在该回路中,AhR是一个关键节点,能够显著放大多胺合成和随后的效应(图5)。
与肿瘤相比,Kyn-多胺-AhR回路的存在在自身免疫中尚不明确。有研究表明,在某些自身免疫性疾病中,所有这些因子都介导了类似的保护作用。如前所述,与对照组相比,给EAE小鼠服用IDO1抑制剂导致疾病进展恶化;相反,另一项研究报告相同酶的正变构调节在相同的神经炎症模型中具有保护作用。此外,Trp代谢产物激活AhR对EAE有保护作用。在Cx3cr1cre -Ahrfl/FLfl小鼠中,通过口服Trp可激活小胶质细胞特异性AhR降低EAE的严重程度。由于亚精胺也能保护小鼠免受EAE的侵袭,犬尿氨酸-多胺-AhR免疫调节回路有助于预防某些自身免疫性疾病。
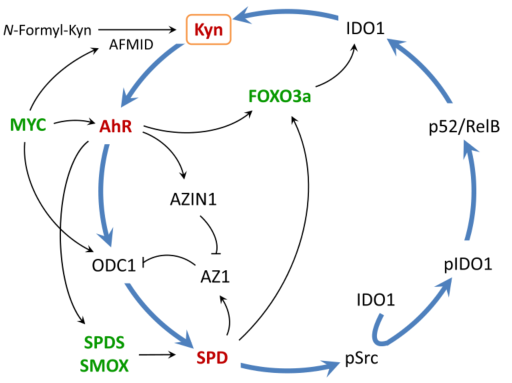
图5 AhR是一种基于Kyn和亚精胺(SPD)的免疫调节电路的中心节点
系统的代谢组学分析研究清楚地表明,这三种多胺和几种AhR配体可以由哺乳动物细胞和肠道微生物群产生。在这方面,这些分子被认为是“共代谢产物”(即微生物群和宿主代谢相互作用产生的化合物),这增加了这些分子生物合成途径的复杂性。肠道中此类共代谢物的主要功能是维持肠上皮屏障,刺激肠胃蠕动,产生肠激素以及调节免疫力和消炎作用,这从小鼠上皮内的CD4+T辅助(Th)细胞转化为Treg淋巴细胞(CD4+CD8αα上皮内淋巴细胞)和抑制Th17细胞极化可以证明。
因此,多胺和Kyn可能通过AhR在体内平衡中相互作用,防止自身免疫反应,从而防止自身破坏。当生理条件变为病理条件时(即通过AhR、IDO1、ODC1、AZIN1、SPDS、SMOX和/或FOXO3a的异常表达),这种免疫调节回路可能决定过度的免疫抑制,从而有利于肿瘤免疫逃逸。事实上,AhR与MYC癌蛋白之间的功能关联支持了这种回路在肿瘤性疾病中的相关性,人类结肠癌细胞中MYC癌蛋白可上调Ahr本身以及编码Trp转运蛋白、芳基甲酰胺酶和ODC1的基因表达。
小结
氨基酸代谢产生多胺(腐胺、亚精胺和精胺)和犬尿氨酸(Kyn),发挥细胞生命所必需的多种功能。多胺代谢失调会导致细胞增殖和分化、信号转导等生物学过程发生改变。特别是亚精胺,在小鼠自身免疫性疾病(包括多发性硬化症和银屑病)模型中具有保护作用。越来越多的证据表明,犬尿氨酸具有多种功能,包括调节免疫和神经反应,调节血管张力,以及小鼠和人类的肿瘤增殖。并且多胺和犬尿氨酸都能抑制抗肿瘤免疫并有助于某些自身免疫疾病的改善。而这些作用都是通过芳香烃受体(AhR)介导和放大的,因此,这种多胺-Kyn-AhR回路及其最关键和最灵活的分子节点的鉴定会为一系列疾病提供新的、更有效的免疫治疗策略。
针对于鸟氨酸、精氨酸、色氨酸及其通路中间代谢物,麦特绘谱开发出Q300全定量代谢组、Q200宏代谢组等分析方法,通过构建每一种标准品标准曲线可绝对定量检测本文中所涉及的代谢物。
参考文献
ElisaProietti et al. Polyamines and Kynurenines at the Intersection of Immune Modulation. Trends in Immunology. https://doi.org/10.1016/j.it.2020.09.007.
原文阅读,请长按识别下方二维码

关于麦特绘谱
麦特绘谱生物科技(上海)有限公司(Metabo-Profile),专注于精准医学和健康领域的代谢组学技术服务,致力于成为全球代谢组学研究者的首选合作伙伴。
麦特绘谱拥有全套高端质谱检测平台,凭借自身在精准医学和健康领域的代谢组学技术及转化经验,研发了靶向定量、代谢芯片、非靶向、代谢流等十几种代谢组学检测方法及科研试剂盒,利用静态及动态分析,来深入解读疾病的病理机制、治疗靶点的发现和验证、药物的作用及毒性研究等,大量的临床研究数据积累为代谢组产业化提供了夯实的基础。
精彩推荐
2. NATURE REVIEWS DRUG DISCOVERY | 色氨酸代谢—最火的疾病治疗靶点成药性如何?
3. Hepatology | AD/ACLF肝硬化患者“聚焦”色氨酸-犬尿氨酸通路
4. Cell Metabolism | 氨基酸如何支持免疫(上)
5. Cell Metabolism | 氨基酸如何支持免疫(下)
6. Nature Medicine | CARD9,肠道菌群和色氨酸互作对结肠炎的影响
7. NATURE COMMUNICATIONS | 肠道菌群相关代谢物生物学功能解读—色氨酸代谢



