在线讲堂
公开课回顾 | 胆汁酸代谢机制及分子调控作用

7月10日晚, 2019年绘谱学堂第二期微信公开课由麦特绘谱资深技术支持王洋博士主讲的《胆汁酸代谢机制及分子调控作用》圆满结束。在此,小编很认真地听课并记录了相关笔记分享给大家,以便您随时温习和查阅,下面请听王博娓娓道来……
结合麦特绘谱技术团队十多年的胆汁酸研究经验,王博在本期绘谱学堂分别从胆汁酸代谢、胆汁酸代谢信号通路、胆汁酸与肠道菌群研究案例三个方面向各位学员做了详细解读,同大家一起探讨体内胆汁酸具体代谢过程,以及作为信号因子及代谢调节因子的胆汁酸通过何种信号通路与肠道菌群相互作用影响疾病的发生和发展。
胆汁酸代谢
按照R1\R2\R3\X位置上基团不同,其亲脂性不同。按照结构还可以将胆汁酸分为初级胆汁酸和次级胆汁酸,或者结合型胆汁酸和非结合型胆汁酸。
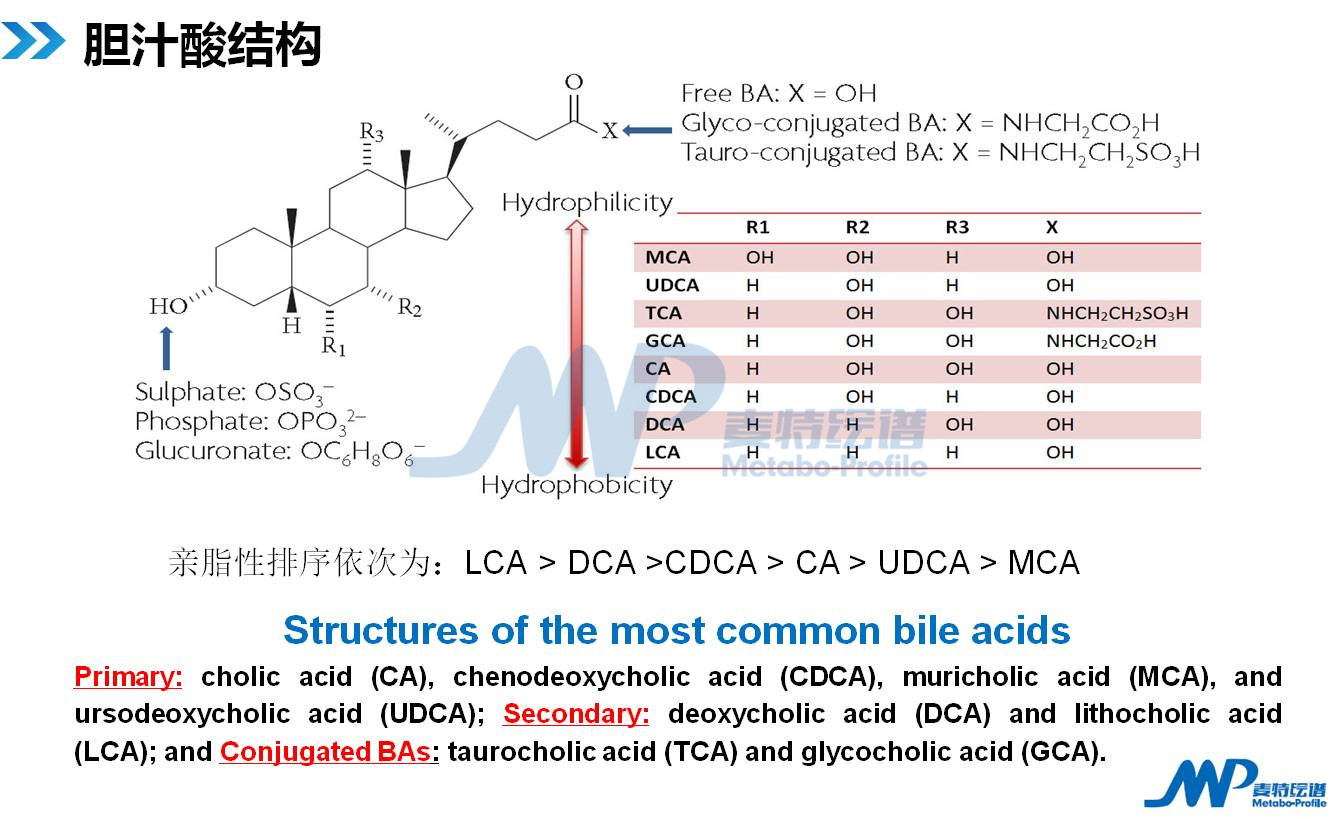
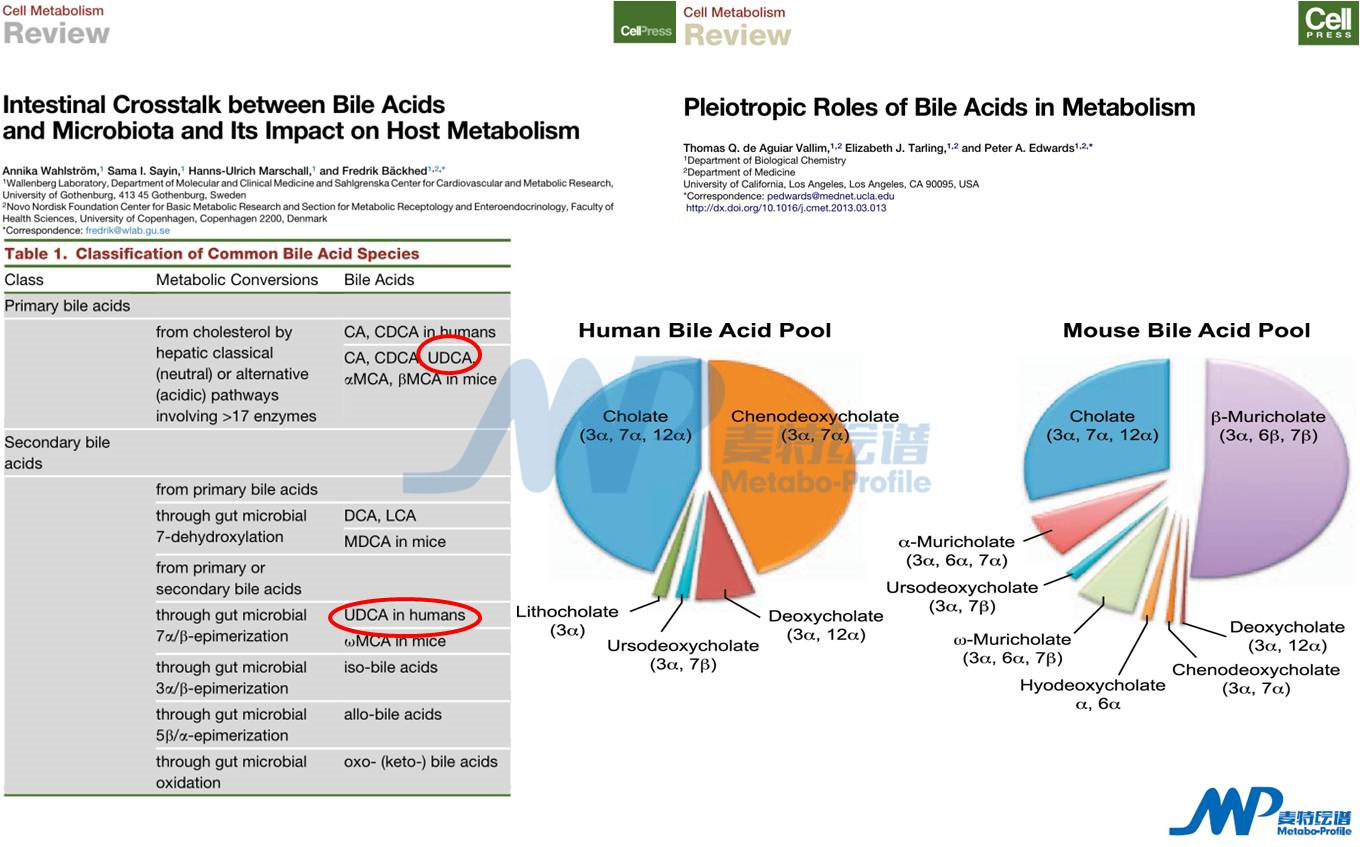
在胆汁酸分类中,有一种胆汁酸需要注意,就是UDCA。UDCA在老鼠体内属于初级胆汁酸,在人体内属于次级胆汁酸。目前有很多胆汁酸分类还不是很清楚。另外,还需要注意的一个问题是人体胆汁酸成分和老鼠胆汁酸成分组成是不一样的。如下图可以看出,人体胆汁酸中CA、CDCA、DCA、LCA等为主,而老鼠胆汁酸中CA、βMCA、ωMCA、αMCA等为主。
胆汁酸代谢比较复杂,涉及的催化反应至少包括了17种不同的酶。肝脏部位,胆固醇通过两种不同途径形成初级胆汁酸。经典途径是胆固醇经胆固醇-7α-羟化酶(CYP7A1)催化生成7α-羟基胆固醇,进一步催化生成胆酸(CA)和鹅去氧胆酸(CDCA),CYP7A1是整条途径的限速酶,决定胆汁酸生成量,在正常条件下至少75%的胆汁酸通过该途径产生。替代途径则由甾醇-27-羟化酶(CYP27A1)催化生成27-羟基胆固醇进一步被氧甾醇-7α-羟化酶(CYP7B1)催化生成CDCA。值得注意的是,替代途径主要产生CDCA,而经典途径产生CDCA和CA,两种初级胆汁酸的比例由甾醇-12α-羟化酶(CYP8B1)决定。除CA和CDCA外,小鼠还产生初级胆汁酸MCAs(主要是β-MCA)和熊去氧胆酸(UDCA)。然后与牛磺酸和甘氨酸进行结合。
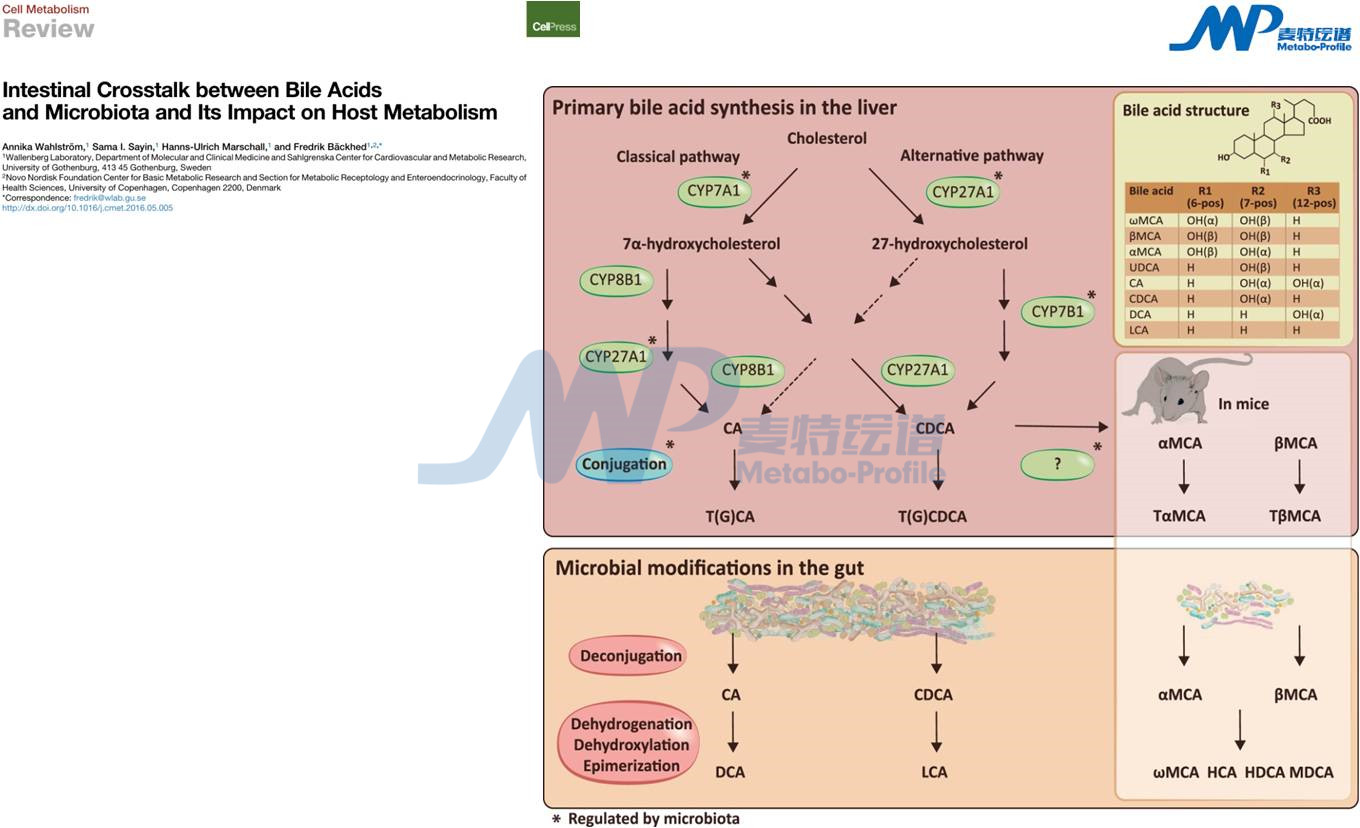
生成初级胆汁酸与牛磺酸和甘氨酸进行结合形成结合型胆汁酸。需要注意的是,人体中胆汁酸主要与甘氨酸结合,而小鼠和大鼠体内胆汁酸主要与牛磺酸结合。非结合型胆汁酸可以通过扩散穿过细胞膜,而结合型胆汁酸需要通过胆盐输出泵(BSEP,也称为ABCB11)主动运输到胆汁中,并储存在胆囊内,随后被释放到十二指肠。同时,也会生成硫酸化胆汁酸或葡糖醛酸化,并与甘氨酸或者牛磺酸进行结合,由多药耐药性相关蛋白2 (MRP2,也称为ABCC2)分泌到胆囊中。当发生胆汁淤积时,大量的胆汁酸和胆红素通过包括MRP3和MRP4在内的MRP家族成员以及钠盐非依赖有机阴离子转运多肽2 (OATP2,也称为SLCO1B1)、有机溶质转运体OSTα-OSTβ异源二聚体转运至循环系统。
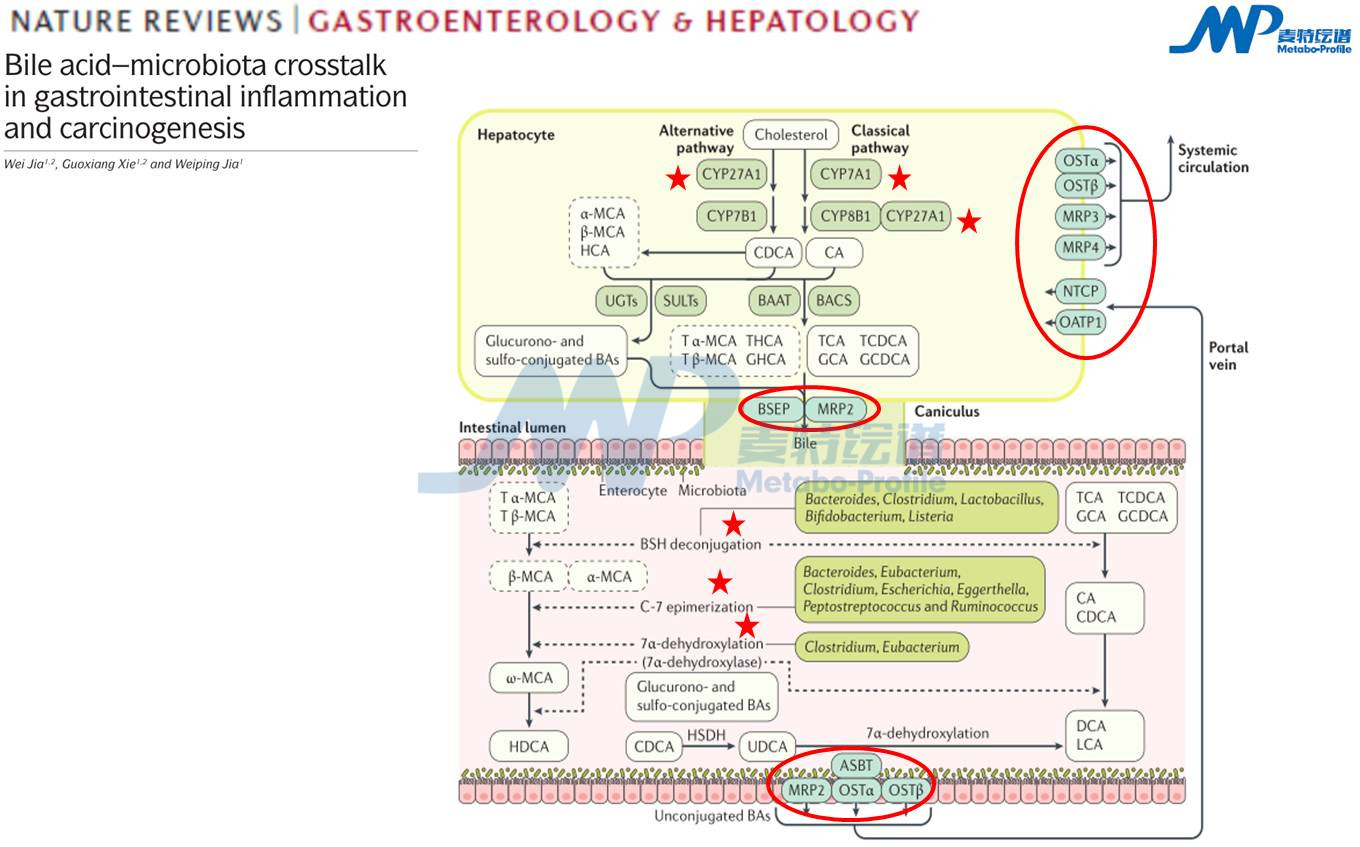
胆囊收缩释放胆汁酸(以胆汁酸、胆固醇和磷脂混合的胶束形式)进入肠道,来自肠道细菌的微生物酶继续代谢胆汁酸,甘氨酸和牛磺酸结合的CA和CDCA通过胆酸盐水解酶(BSH)去结合和7α-脱羟基形成次级胆汁酸(DCA和LCA)。Tα-MCA和Tβ-MCA通过胆酸盐水解酶(BSH)形成α-MCA,β-MCA。β-MCA通过C-7差向异构化形成ω-MCA,再经7α脱羟基形成猪去氧胆酸(HDCA),经过7β-差向异构化形成猪胆酸(HCA,也称为γMCA)。
胆汁酸去结合过程由具有胆盐水解酶(BSH)活性的细菌主导的,参与胆汁酸代谢的肠道菌属主要有:拟杆菌、梭菌、乳酸菌、双歧杆菌、利斯特氏杆菌等参与胆汁酸去结合;拟杆菌、梭状芽孢杆菌、大肠杆菌、埃格菌、优杆菌、消化性链球菌和瘤胃球菌主要参与C3、C7和C12羟基的氧化和差向异构化;梭状芽胞杆菌和优杆菌参与7-去羟基化;拟杆菌、优杆菌和乳酸菌参与酯化反应;梭状芽孢杆菌、梭杆菌、胃球菌和假单胞菌参与脱硫过程。
在回肠末端,大多数非结合胆汁酸(包括CA、CDCA DCA, UDCA HDCA,α-MCA,β-MCA,和ω-MCA)经顶端钠依赖性胆汁酸转运体(ASBT) 、MRP2等吸收进入肠上皮细胞,并分泌到门静脉。经过循环系统到达肝脏,由肝细胞钠/牛磺胆酸盐转运多肽(NTCP)和有机阴离子转运多肽1 (OATP1)进入肝细胞。临床上,NTCP主要负责结合胆汁酸的摄取(>80%),而OATP家族成员主要将未结合或硫酸化胆汁酸运输到肝脏。这样就完成了一次肝-肠循环。每天胆汁酸池90–95%胆汁酸进行循环,一天肠道和肝脏之间循环次数大约6-10次,每天只产生约0.2~0.6克的新合成胆汁酸,以维持一个稳定的胆汁酸池。
通过胆汁酸代谢通路展示图可以看出,我们可以通过几个方面对胆汁酸进行分析:1)胆汁酸各成分组间变化规律,胆汁酸比例变化规律,不同种类(初级和次级、结合和非结合等)胆汁酸变化规律;2)胆汁酸代谢酶变化规律(如CYP7A1、CYP27A1、CYP8B1);3)胆汁酸转运重吸收等受体表达变化规律(如BSEP、MRP2、ASBT)。
胆汁酸代谢信号通路
胆汁酸是如何发挥信号分子作用的呢?其实主要依赖于两种关键的受体,一种是法尼醇X受体(FXR),它是核受体的一种,另外一种是G蛋白偶联受体(TGR5)。
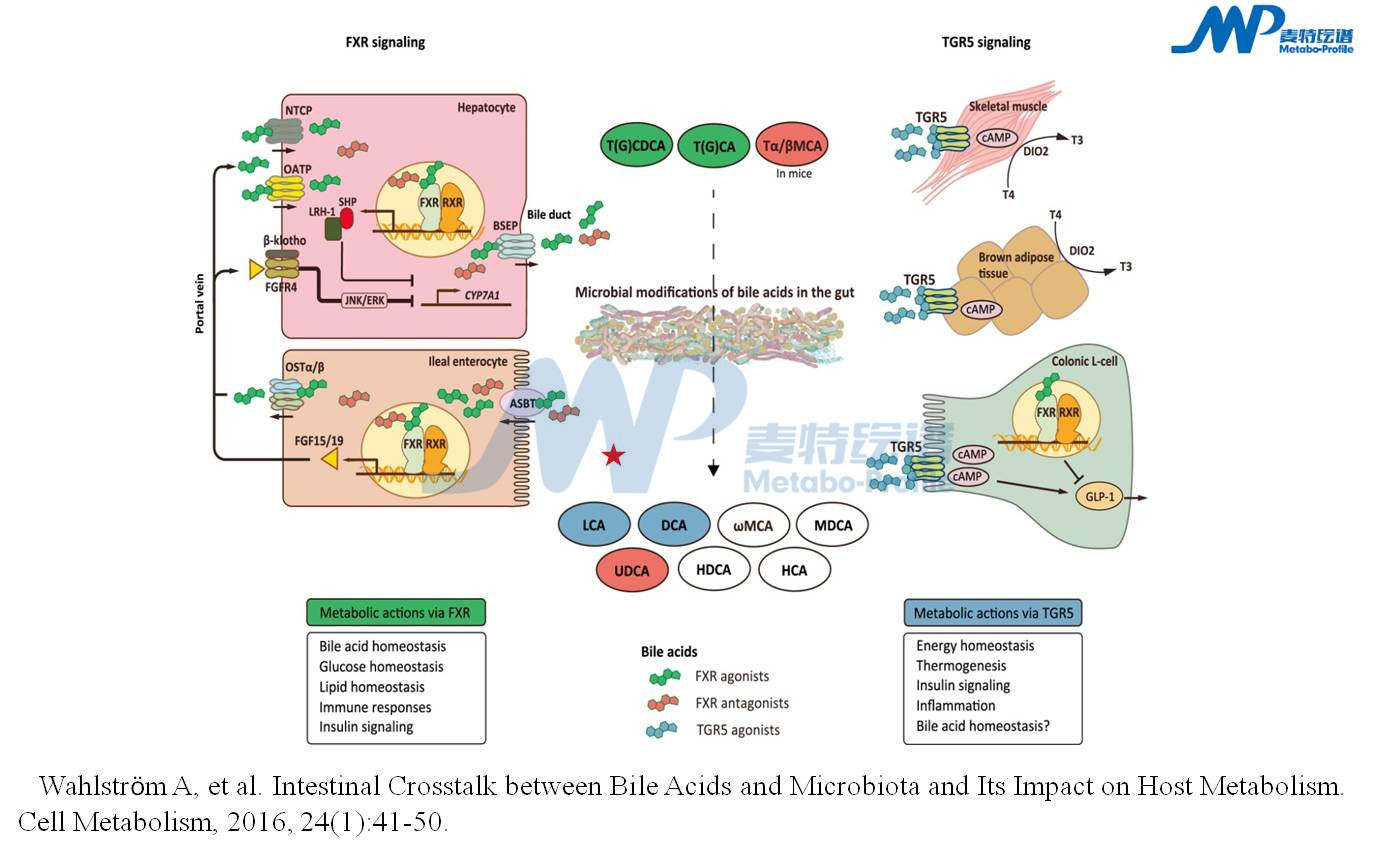
FXR在多种组织中均有表达。其中研究最多的部位是肝脏和回肠。肝FXR是胆汁酸合成和肝内循环的主要调节因子。在正常生理条件下,肝脏FXR主要调节胆道系统和肠道的胆汁酸水平,限制胆汁酸在肝脏中的积累。肠道FXR维持胆汁酸回流到门静脉,并控制胆汁酸再摄取进入肠细胞,从而限制细胞内胆汁酸水平。远端回肠肠细胞重吸收胆汁酸,胆汁酸激活或抑制FXR活性,诱导小鼠FGF15或者人体FGF19表达。FGF15 /19通过门静脉到达肝脏,与FGF受体4(FGFR4)/b-klotho异二聚体复合物结合,触发JNK1/2和ERK1/2信号级联反应影响Cyp7a1的表达,最后调节胆汁酸的合成代谢。另外,胆汁酸激活肝脏FXR诱导小异二聚体伴侣(SHP)分子的表达,SHP与肝受体同源蛋白-1 (LRH-1)结合,从而抑制Cyp7a1基因的表达。此外,FXR还可以诱导其他转运体BSEP/ABCB11、 MDR3/MDR2/ABCB4、ABCG5/ABCG8的表达影响胆汁酸代谢。TGR5主要由疏水性次级胆汁酸LCA和DCA激活,是微生物与胆汁酸相互作用的另一个靶点。TGR5的激活导致受体内化,环磷腺苷(cAMP)水平升高,蛋白激酶A活化,导致靶蛋白磷酸化水平增加,这种活化引起的结果是广泛的且具有细胞特异性,最终引起褐色脂肪组织能量消耗,改善葡萄糖代谢和胰岛素敏感性,增加肠道运动等变化。此外,胆汁酸其他受体包括孕烷X受体PXR、维生素D受体。因此我们可以针对胆汁酸变化,选择信号通路上的各个指标进行检测分析。

案例分享
第一个案例为胆汁酸与阿尔兹海默症之间的研究
该研究纳入1464例样本,其中认知正常370例,早期轻微认知障碍284例,晚期轻微认知障碍505例以及AD病人305例。首先确定不同阶段人群胆汁酸是否发生变化,且这种变化与认知能力下降是否相关,MCI进展到AD患者中,CA水平下降,而GDCA/CA、TDCA/CA水平均上升,提示它们是评价MCI进展的标志物群。其次,对BAs与ATN (β-淀粉样蛋白,tau蛋白,神经退化)三种疾病生物标志物相关性进行分析;此外,结合基因检测,进行胆汁酸与风险基因位点相关性分析。这个案例是从临床角度出发,挖掘胆汁酸在临床辅助诊断、评估中的应用。

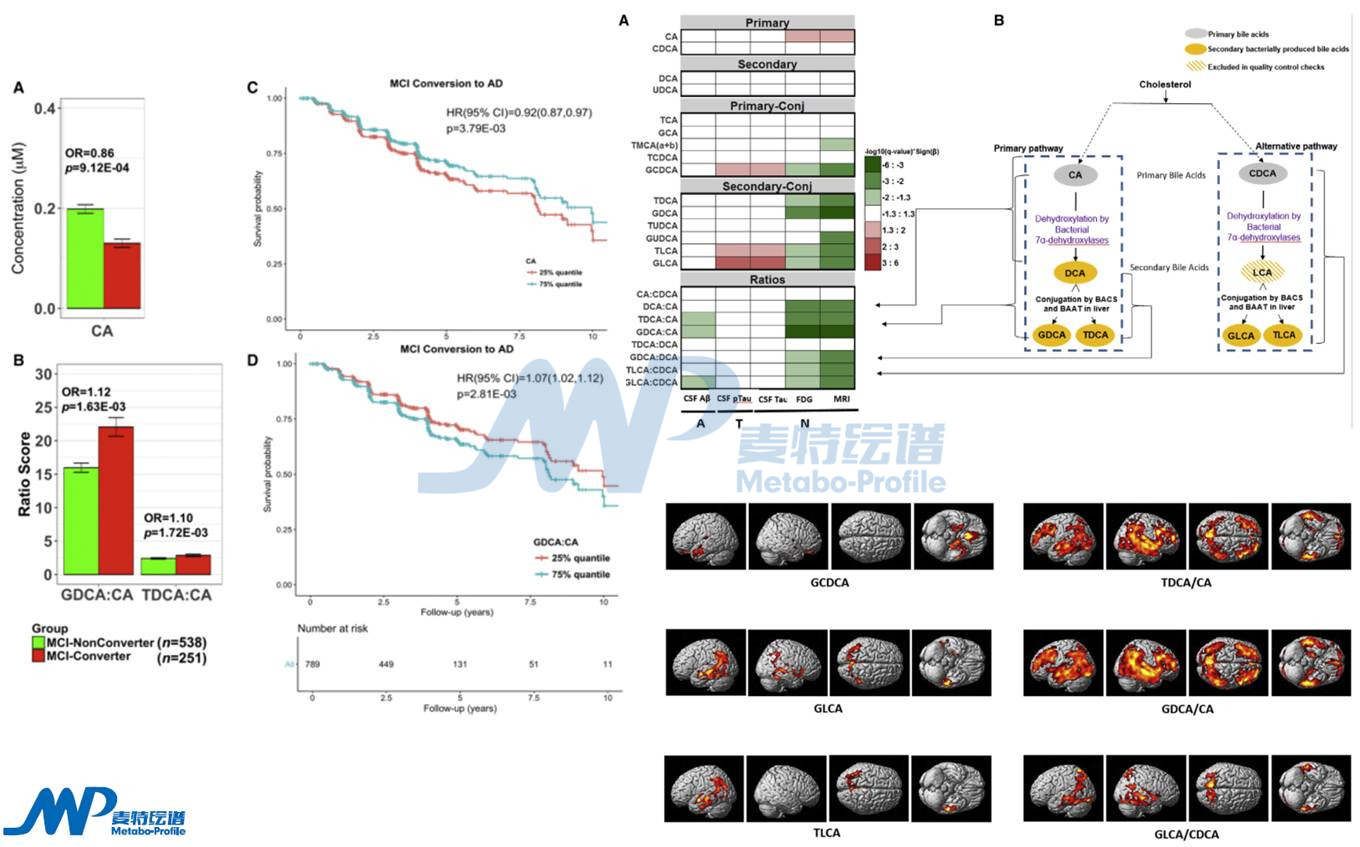
案例详细解析请点击查阅:胆汁酸或将成为阿尔茨海默病新的生物标志物
第二个案例从胆汁酸和肠道菌群角度研究二甲双胍药效机制研究

对二甲双胍治疗前后肠道菌群进行检测分析,发现短期给予二甲双胍就能够明显的引起肠道菌群重塑,其中脆弱拟杆菌丰度显著被抑制。通路分析发现次级胆汁酸代谢受到影响。随后采用代谢组学分析了粪便、血清中胆汁酸变化规律,其中TUDCA\GUDCA水平显著变化。随后对FXR等信号通路进行检测分析,发现肠FXR在二甲双胍干预之后,明显被抑制,而肝FXR却没有显著改变。进一步证实GUDCA是肠FXR内源性拮抗剂。将筛选到的脆弱拟杆菌进行灌胃,发现脆弱拟杆菌可以逆转二甲双胍降糖作用。而补充GUDCA,糖尿病模型小鼠体重明显减轻,血糖明显改善,胰岛素敏感性也增加了,能够有效的治疗糖尿病。
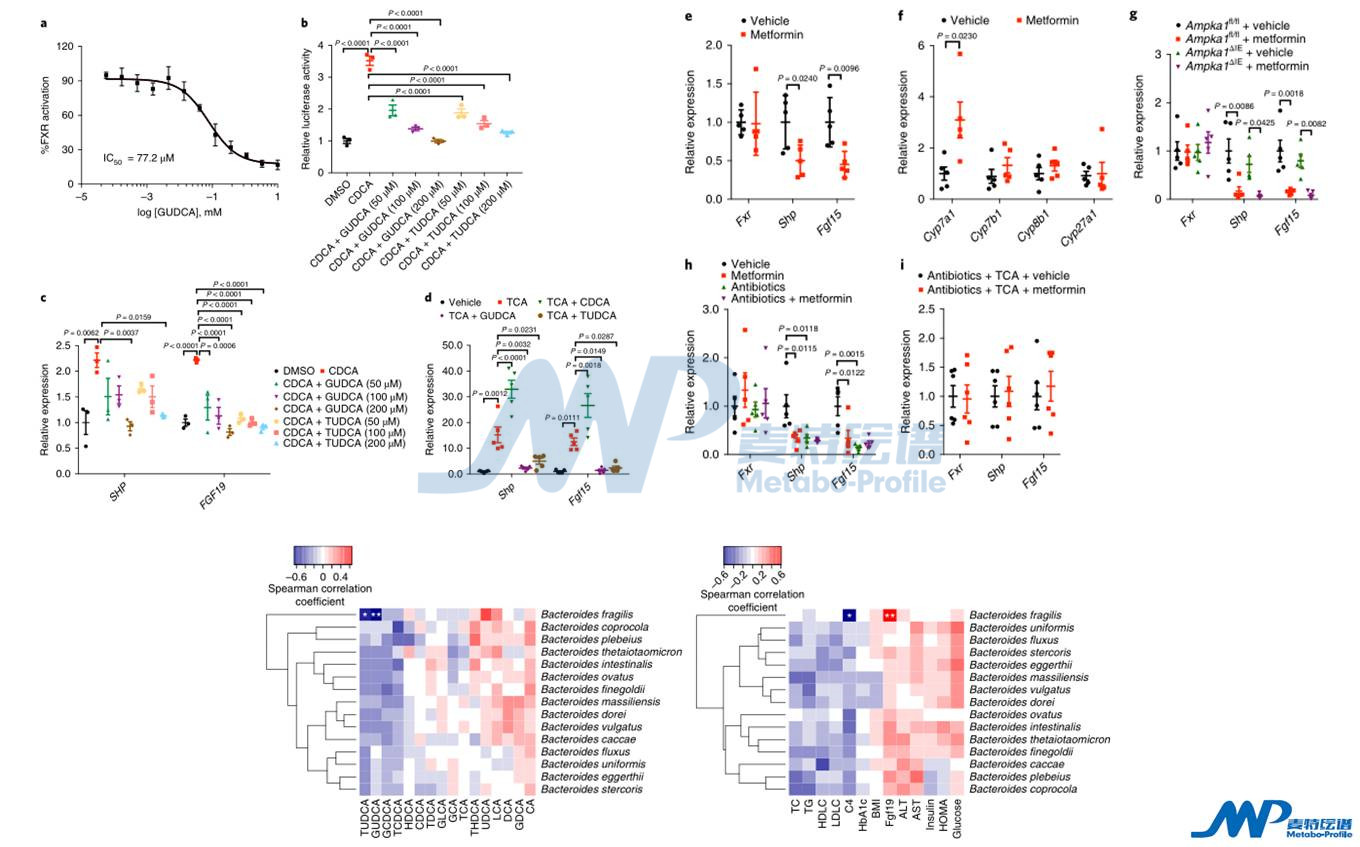
案例详细解析请点击查阅:Nat. Med. | 二甲双胍通过调节肠道菌群与胆酸代谢改善葡萄糖代谢疾病
胆汁酸相关药物研发情况
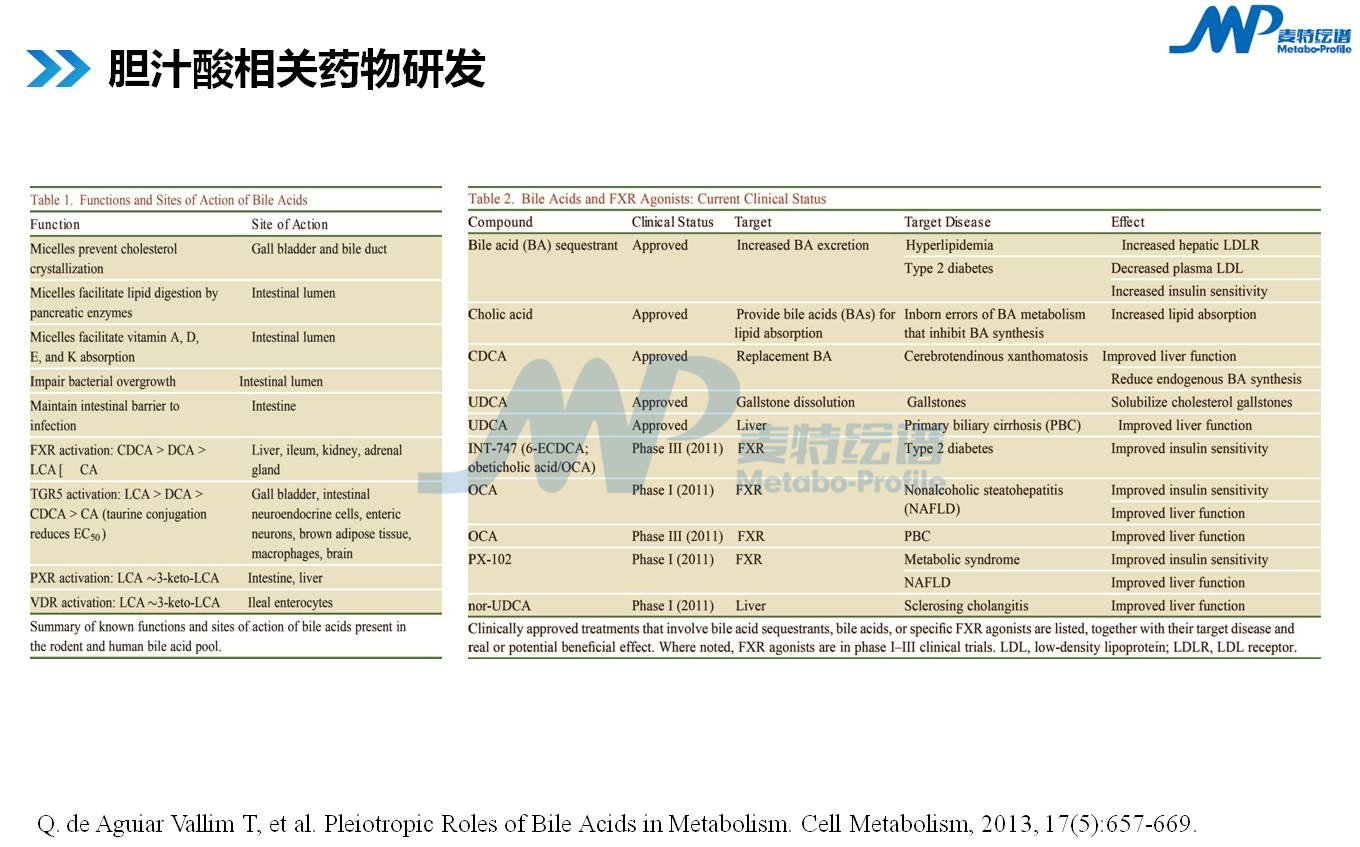
胆汁酸的信号通路疾病当中发挥极其重要的作用,是药物干预的一类靶点。以下突变为胆汁酸的几种药物的研发情况。主要有CDCA及其衍生物、UDCA及其衍生物、胆汁酸螯合剂(如消胆胺)及胆汁酸转运体ASBT抑制剂。
麦特绘谱主要产品服务

Q&A
Q1: 做了非靶向代谢组,发现两种胆汁酸出现显著差异,想对这两种胆汁酸进一步分析,有什么建议呢?
A:非靶向代谢筛选出的差异物还需要进一步验证,如果该疾病与胆汁酸相关性比较强,可以对胆汁酸谱进行靶向绝对定量验证一下,根据验证结果进行后续验证方案设计。
Q2:胆汁酸对肠道中菌群中哪类菌群影响最大?
A: 胆汁酸和肠道菌群相互影响。其中拟杆菌、梭菌、乳酸菌、双歧杆菌、等参与胆汁酸去结合;拟杆菌、梭状芽孢杆菌、大肠杆菌、瘤胃球菌等参与羟基氧化和差向异构化;梭状芽胞杆菌和优杆菌参与7-去羟基化;拟杆菌、优杆菌和乳酸菌参与酯化反应;梭状芽孢杆菌、梭杆菌、胃球菌和假单胞菌参与脱硫过程。可以通过饮食补充胆汁酸考察某种胆汁酸对菌群的影响。
Q3: 临床及动物模型均显示肝损失后,总甘油三酯和总胆汁酸存在显著性差异,该如何进行下一步研究?
A: 可以针对胆汁酸谱进行检测分析,临床上可以进行血清、粪便两种样本胆汁酸检测;动物实验可以对血清、肝脏、肠内容物进行检测,先选择哪种样本进行分析则需要根据研究目的进行选择。目前已经有文献报告肝损伤中胆汁酸成分会出现明显变化。
Q4: 粪便和血清中胆汁酸分别反映哪些部位胆汁酸含量?肝脏疾病是不是要特意检测肝脏中胆汁酸?
A: 粪便胆汁酸表征由肝脏转运至肠道的环节(肠道胆汁酸升高可能是肠道重吸收受阻或者肝脏分泌过多)、血清表征整体状态(血清胆汁酸过多可能是肠道重吸收增加,也有可能是肝脏胆汁酸淤积)、肝脏部位主要还是表征胆汁酸合成。三个部位全部分析才会更系统的阐述清楚哪个部位的功能出现异常。
Q5: 研究肠道肿瘤和胆汁酸的关系时,粪便和血液胆汁酸优选哪一个?
A: 如果从机制方面进行研究可以选择粪便胆汁酸,同时可以对菌群去进行检测,两部分结果可以进行相关性分析,探讨群菌-胆汁酸-疾病三者之间的关系。如果寻找生物标志物,血清会更好一些,临床方面收集血样更方便。选择哪种样本,还是要根据研究目的进行判断。



