文献解读
Cell | ASICs介导肠道5-羟色胺能神经元调控线虫觅食行为
本公众号在《胆汁酸或将成为阿尔茨海默病新的生物标志物》一文中提到大脑和肠道之间双向生化信号传导对各种神经退行性疾病和精神疾病具有一定作用。当处于饥饿状态时,神经系统如何感知食物摄取来驱动行为?肠道信息如何回传至大脑?麻省理工大学Steven W. Flavell团队对秀丽隐杆线虫(Caenorhabditis elegans,C. elegans)消化道如何给大脑发送信号从而改变线虫的觅食行为进行了系统研究,相关研究结果发表于《Cell》期刊上。
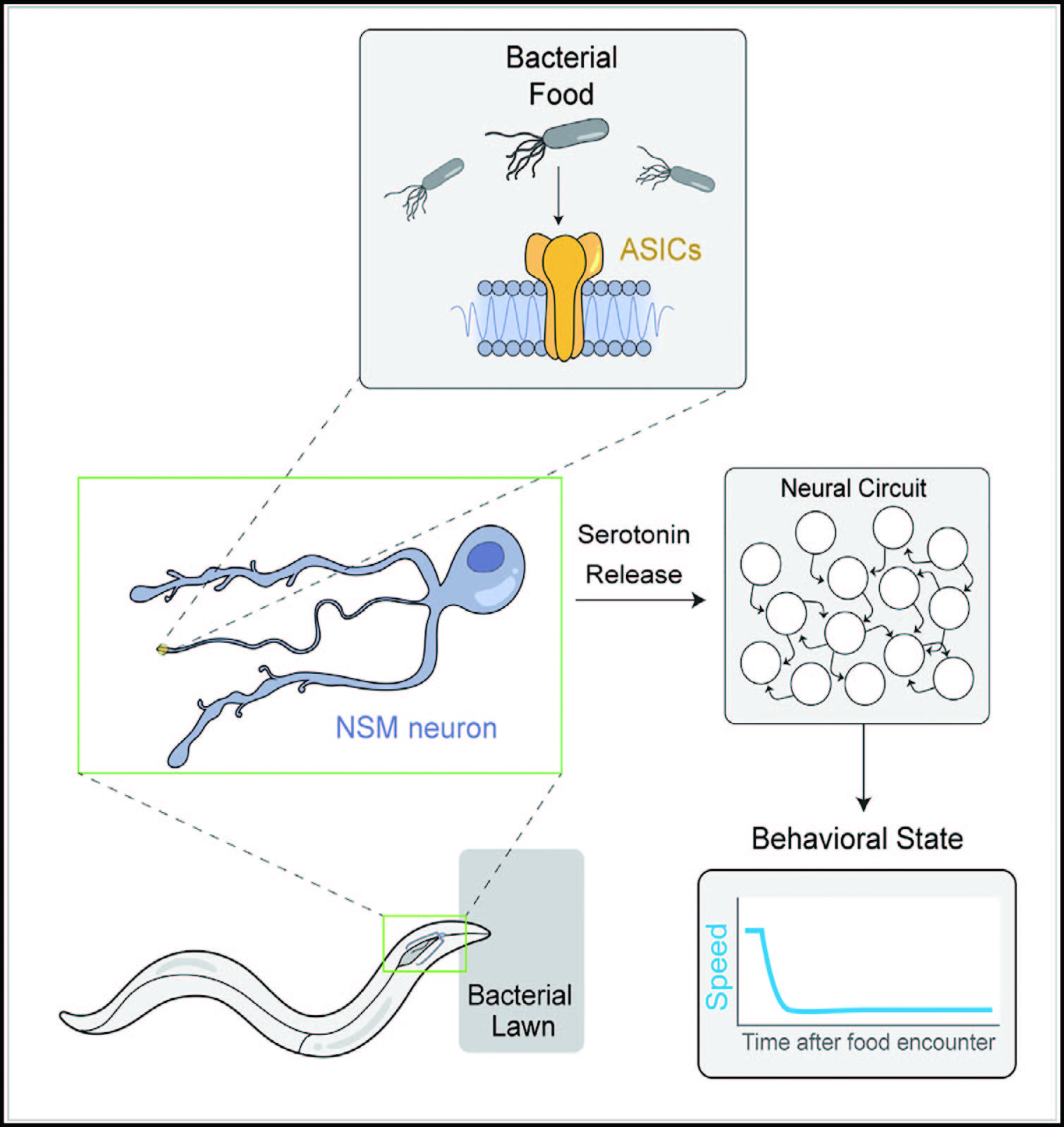
所有动物必须通过产生适应性行为来响应食物的摄入。肠内分泌细胞和肠神经系统神经元分布在胃肠道(GI),并在调节食物摄入的反应中起关键作用。 这些细胞在监测消化道内容物和调节GI运动、分泌等局部过程中具有感受器作用。它们还可支配肠道迷走神经感觉神经元的动作向CNS发出信号。目前普遍认为,肠道-大脑信号可能对调节内心状态如情绪和食欲很重要,来自肠道的信号让我们知道什么时候吃饱了,大脑通过瘦素和生长激素来帮助我们控制食欲。但目前对肠道神经元如何检测摄食欲望以及影响CNS回路产生复杂神经活动模式的理解不足。比如5-羟色胺(5-HT)对健康很重要,但是5-羟色胺在肠道影响摄食行为中的作用不清楚,即使在CNS中,5-HT的作用也没有完全明确。已知C. elegans神经系统中5-HT等神经调节剂可调节与摄食有关的行为。例如,研究者发现,当C. elegans遇到食物时,它们会放慢移动速度来吃掉食物,吃饱后又开始四处游荡。5-羟色胺释放参与线虫移动减慢这个过程,却不清楚是什么触发了5-羟色胺释放。Steven W. Flavell团队针对一种负责生产5-HT的肠神经元——神经分泌运动神经元(NSM)展开研究。
NSM: 一种肠血清素激活的神经元感知食物消化
NSM位于线虫消化器官咽(pharynx)的内层,当线虫摄入细菌性食物时,NSM神经元会立即激活。NSM神经元具有长长的投射到线虫肠道中的神经突(neurite)(Figure 1A)。这种神经突起充当了NSM神经元的感觉末梢,在线虫摄入细菌性食物时起着激活这些神经元的关键作用。当C. elegans暴露于食物中时,NSM表现出与移动减缓相关的钙离子信号峰。为了测试由食物引起的NSM钙瞬变是否需要突触输入NSM,研究者对unc-13(s69)突变体的NSM活性进行研究,数据结果表明,即使减弱突触和神经肽输入,NSM仍会通过钙瞬变产生获取食物的响应。而NSM表现出摄食依赖活性的前提是必须成功摄入细菌类食物,并且细菌膜热不敏感组分是激活NSM活性的必要条件,单纯的机械刺激也不会激活NSC活性。总的来说,NSM以不需要突触或神经肽输入的方式响应细菌食物的摄入。

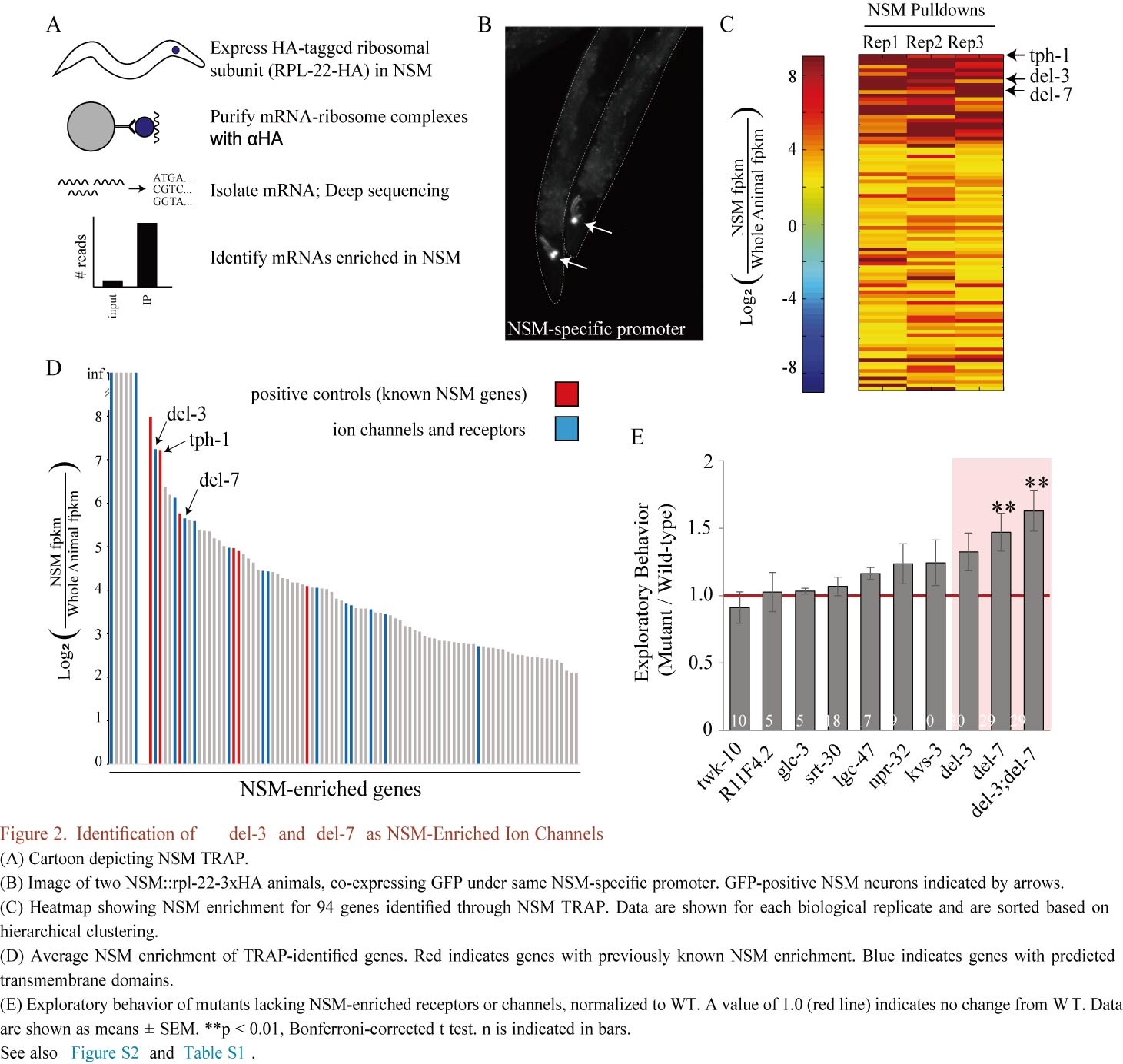
进一步研究结果揭示出两个新的位于神经突最顶端的离子通道被称为DEL-3和DEL-7,是NSM神经元被摄入的细菌性食物激活所必需的(Figure 2,Figure 3)。这两种离子通道属于酸敏感离子通道(acid-sensing ion channel, ASIC)蛋白家族。ASIC存在于包括人类在内的所有动物中,在味觉和疼痛检测方面起作用,而其他功能仍然未知。有趣的是,这些蛋白在哺乳动物肠道肠神经元中也有表达。因此ASIC可能在检测存在于消化道和其他地方的细菌群体中发挥着重要作用。DEL-3和DEL-7如何感知细菌?可能是这两种离子通道直接检测细菌分泌的化合物,也可能是细菌化合物与附近的受体相互作用,随后激活这两种离子通道。另外,线虫食物摄取引起的减速是由食物摄入、气味/气体等感官变化,还是两者相互作用引起的尚不清楚。研究结果显示DEL-3和DEL-7在进食诱导行为放缓中发挥重要作用(Figure 4),当接近食物时,DEL-3和DEL-7在其他细胞中起作用以减缓运动,但在NSM中必须要接触食物后才会减缓运动。一旦NSM细胞的离子通道被激活,细胞就开始分泌5-羟色胺,然后就会被附近表达5-羟色胺受体的神经元检测到,这表明食物摄取与5-HT依赖性减慢移动相关。
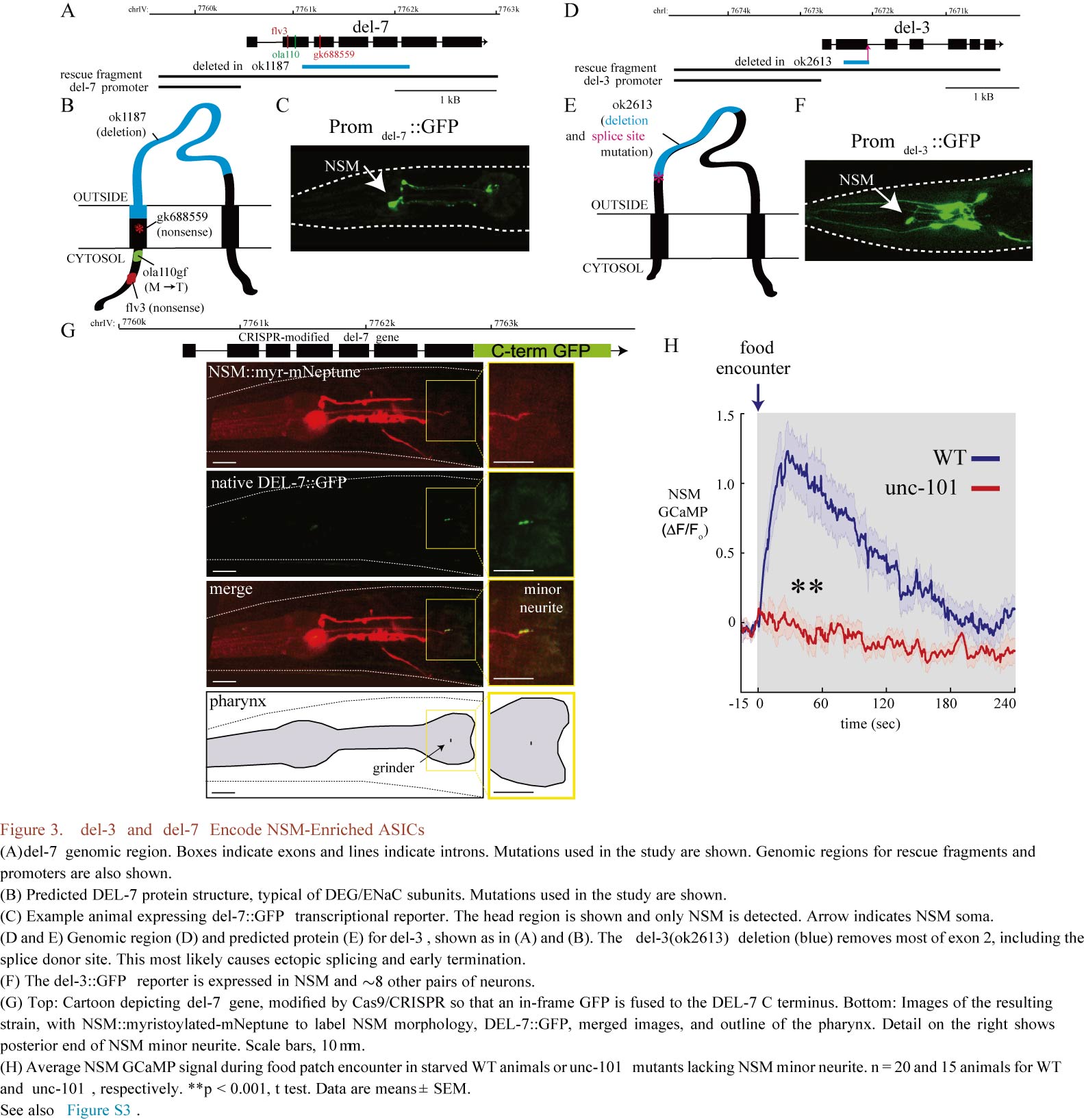
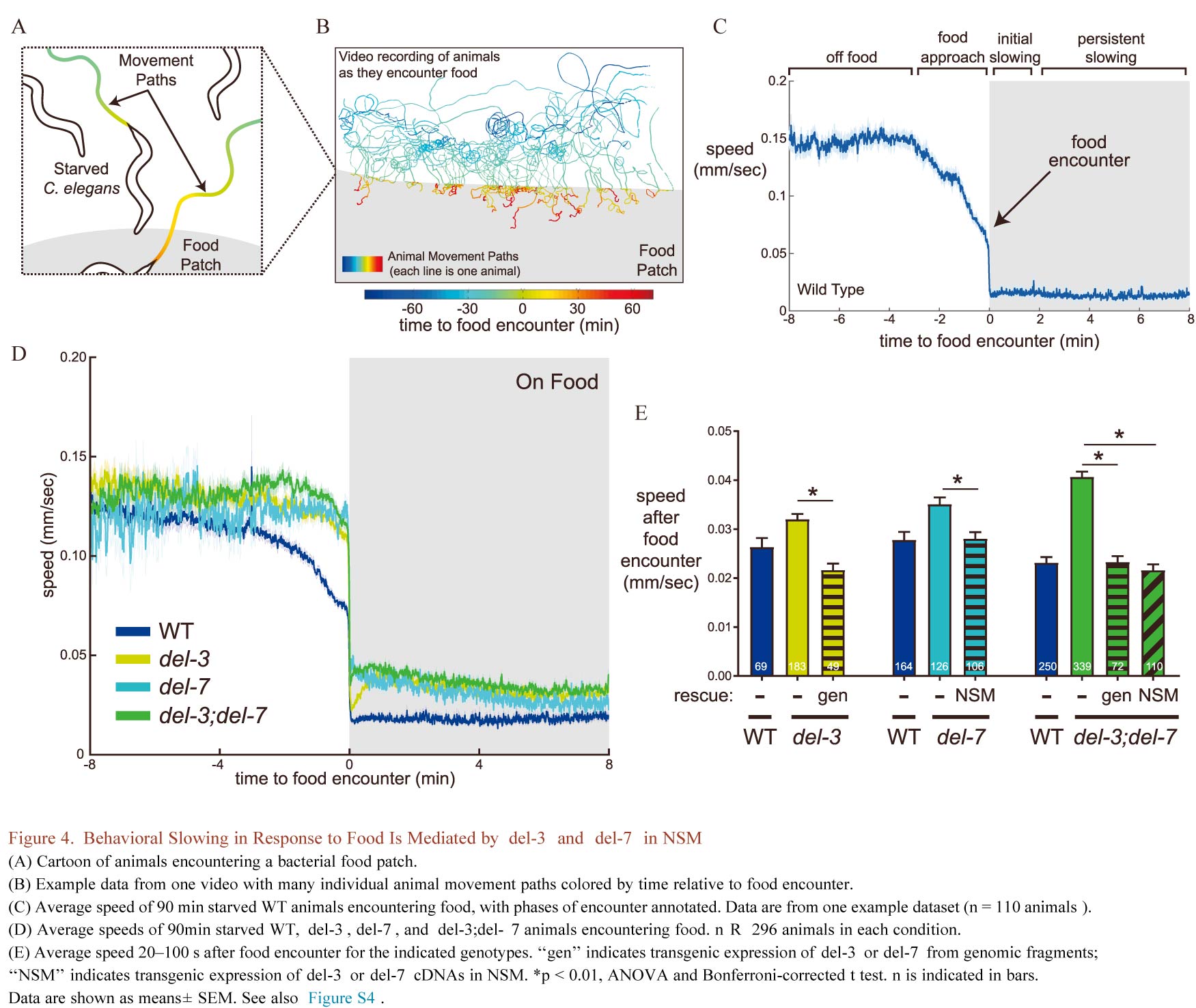
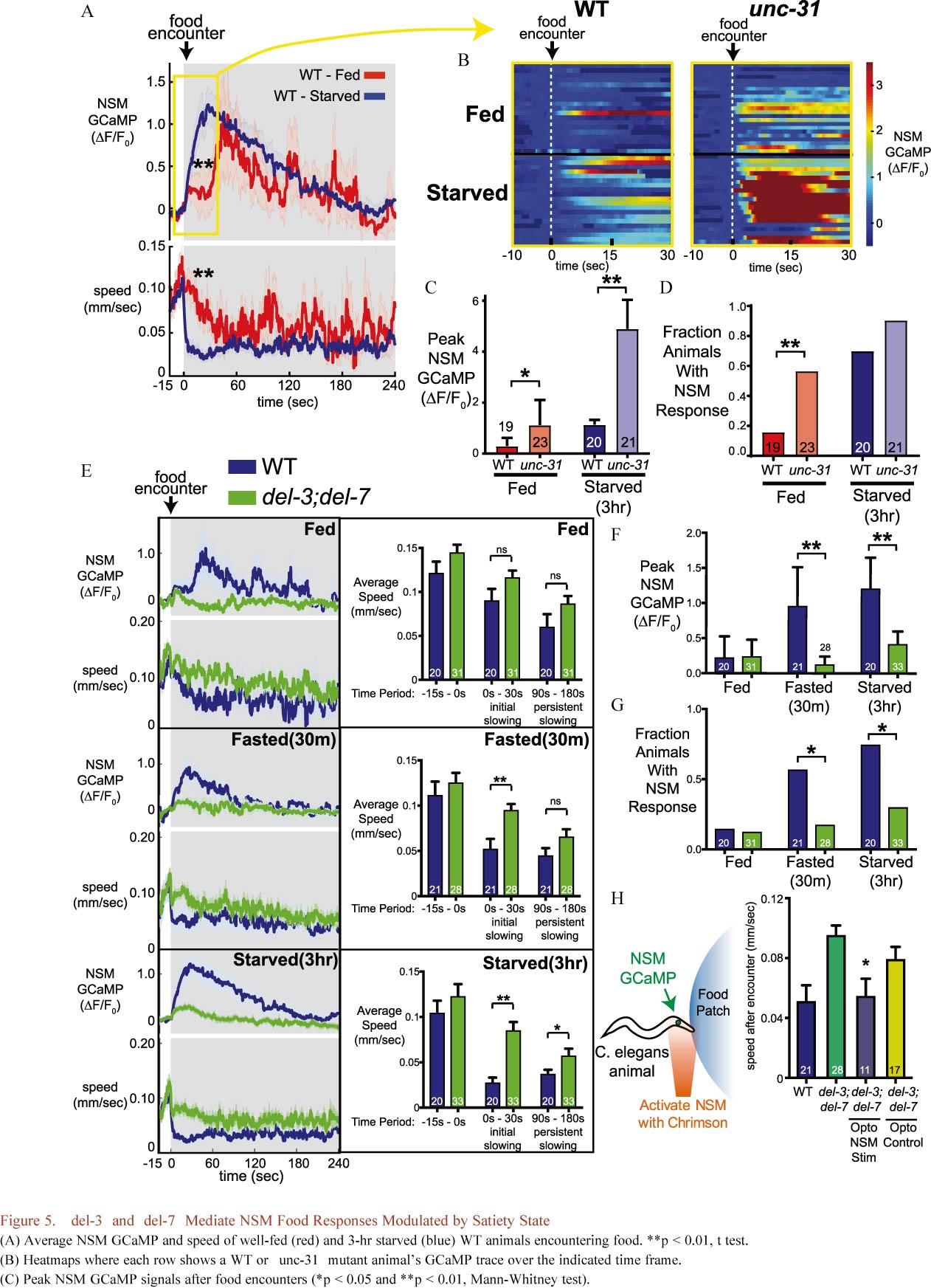
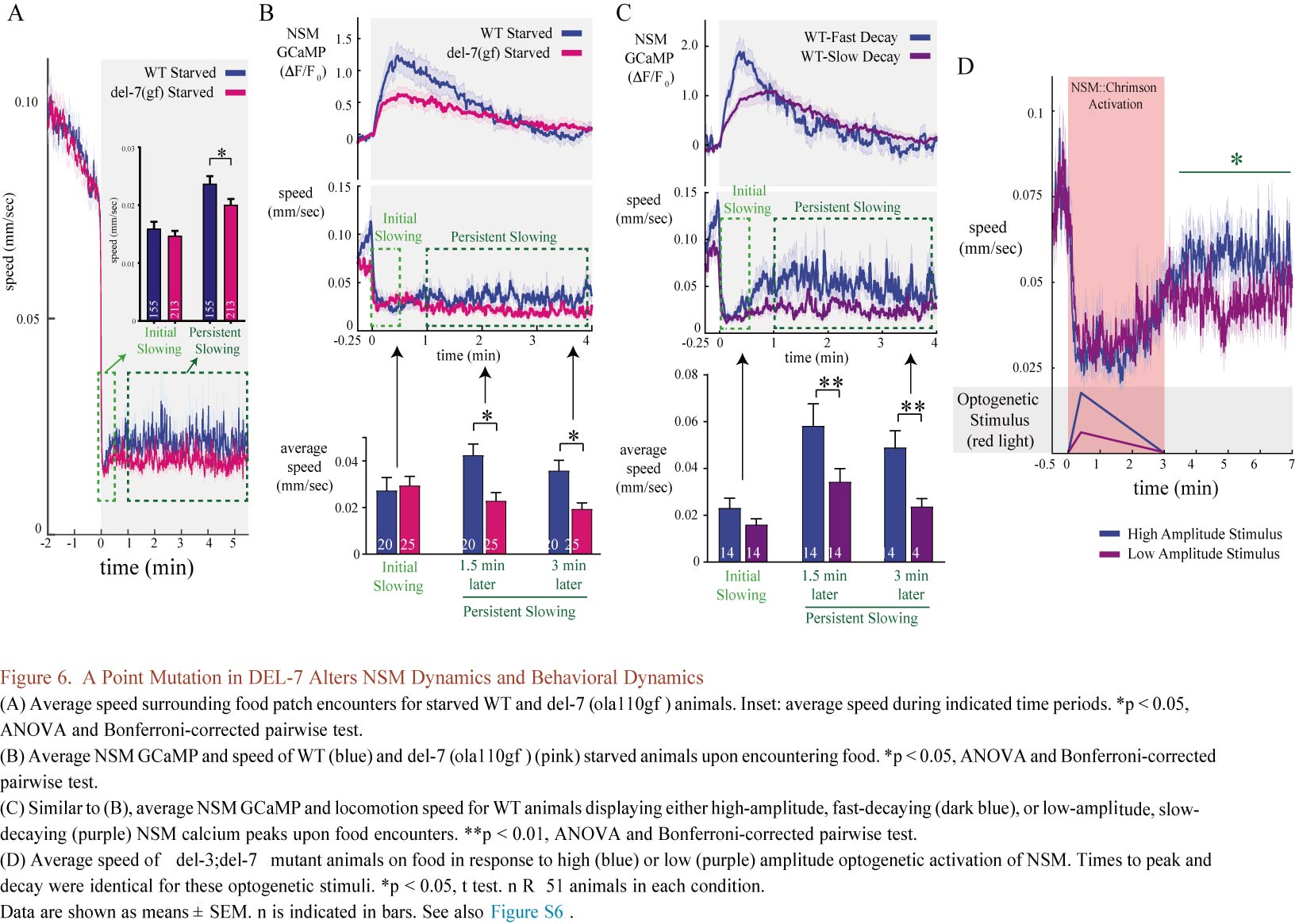
作者又分别针对饥饿状态、饱腹状态下C. elegans是否保持一致的信号传导展开研究,结果表明NSM对食物摄入的反应受饱腹感调节:饥饿动物NSM食物摄入后立即被激活,而在喂养良好的动物中被抑制,直到其活性在喂养后期被解除(Figure 5)。DEL-7和DEL-3作为NSM富集的通道,这些通道需要依赖于摄食的NSM活动,这反过来驱动动物进食时的缓慢运动。DEL-7通道突变也会改变NSM动力学和相关生物体行为动力学(Figure 6)。
小结
本研究发现线虫肠道中一类神经元专门用于监测线虫何时摄入细菌,一旦这种情形发生,这些神经元就释放一种神经递质,这种神经递质给大脑发出停止移动的信号,并在这种特定的神经元中发现新的用于检测细菌的离子通道(DEL-7和DEL-3)。但另一个悬而未决的问题是,线虫感应细菌的基本机制是否也适用于人类。人类肠道中含有各种各样的细菌,肠道内排列着被称为肠嗜铬细胞的神经元样细胞,这些细胞也可以生产5-羟色胺,并将它们传递给大脑感官神经元。未来研究思路可能旨在5-羟色胺、肠-脑信号如何改变哺乳动物行为,在线虫中的新发现可以为肠-脑轴相关研究提供新的见解。
参考文献
Makki K, Deehan EC, Walter J, et al. The Impact of Dietary Fiber on Gut Microbiota in Host Health and Disease. Cell 176, 1–13 January 10, 2019.



